Хімія. Комплексна підготовка до ЗНО і ДПА
Завдання сертифікаційної роботи з хімії 2018 р. (зошит 1)
Завдання 1-36 мають чотири варіанти відповіді, серед яких лише один правильний
1. Проаналізуйте твердження щодо речовини, структурну формулу якої наведено.
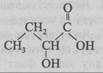
I. Молекулярна формула речовини С4Н8О3.
II. У речовині масова частка Гідрогену найбільша.
- А правильне лише І
- Б правильне лише II
- В обидва правильні
- Г немає правильних
2. Помилковим є твердження, наведене в рядку
- А Електронегативність Сульфуру менша, ніж електронегативність Оксигену
- Б В атомі Оксигену стільки само енергетичних рівнів, як і в атомі Сульфуру
- В Радіус атома Сульфуру більший, ніж радіус атома Оксигену
- Г Окисні властивості кисню виражені сильніше, ніж сірки
3. Укажіть нуклонне число А нукліда Ферум-56, число його протонів Z і нейтронів N.
|
А |
Z |
N |
|
|
А |
56 |
26 |
30 |
|
Б |
26 |
30 |
56 |
|
В |
56 |
30 |
26 |
|
Г |
26 |
56 |
30 |
4. Формули лише йонних сполук записано в рядку
- A Na2S, SO3, H2S
- Б КСl, ССl4, СН4
- В К2О, КОН, КСl
- Г Na2O, РН3, НВr
5. Проаналізуйте з погляду окиснення-відновлення хімічну реакцію, схема якої
NO + NaOH → NaNO2 + N2O + Н2О
У цій реакції Нітроген
- А лише окиснюється
- Б лише відновлюється
- В не змінює ступінь окиснення
- Г і окиснюється, і відновлюється
6. У кристалізатор з водою додали кілька крапель фенолфталеїну й помістили туди шматочок натрію. Він плавиться, перетворюючись на кульку, яка швидко рухається поверхнею води. Одним з продуктів реакції є газувата займиста речовина.
Проаналізуйте твердження щодо реакції, її реагентів і продуктів, зовнішніх ефектів.
I. Реакція є екзотермічною.
II. Густина натрію більша, ніж густина води.
III. Газ, що виділяється внаслідок реакції, — кисень.
IV. Розчин поступово набуває малинового кольору.
Правильні з-поміж них лише
- А I, II
- Б I, IV
- В II, III
- Г III, IV
7. Які речовини реагують між собою у водному розчині з утворенням осаду?
- А купрум(ІІ) сульфат і магній хлорид
- Б купрум(ІІ) сульфат і натрій гідроксид
- В сульфатна кислота і натрій гідроксид
- Г сульфатна кислота і калій карбонат
8. Колір вологого універсального індикаторного папірця змінюється на синій під дією газуватої речовини, формула якої
- А НВr
- Б SO2
- В NH3
- Г H2S
9. Які оксиди реагують між собою?
1. CO2 i Na2O
2. СаО і Na2O
3. СаО і SiO2
4. СО2 і SiO2
- А 1, 3
- Б 1, 4
- В 2, 3
- Г 2, 4
10. Правильне твердження щодо купрум(ІІ) гідроксиду наведено в рядку
- А є сильним електролітом
- Б за нагрівання розкладається
- В легко окиснюється киснем повітря
- Г отримують взаємодією металу з водою
11. Сульфатна кислота реагує з
1. магній карбонатом
2. карбон(IV) оксидом
3. магній гідроксидом
4. силіцій(ІV) оксидом
- А 1, 3
- Б 1, 4
- В 2, 3
- Г 3, 4
12. Окисно-відновною реакцією є термічне розкладання
- А калій гідрогенкарбонату
- Б кальцій карбонату
- В амоній хлориду
- Г натрій нітрату
13. В одній пробірці міститься розчин магній хлориду, в іншій — розчин алюміній хлориду. Відрізнити вміст однієї пробірки від вмісту іншої можна за допомогою розчину
- А сульфатної кислоти
- Б аргентум(І) нітрату
- В калій гідроксиду
- Г калій сульфату
14. В пробірці І міститься розчин натрій карбонату, а в пробірці II — розчин натрій сульфату. В обидві пробірки додали розчин речовини X. Унаслідок цього утворився осад в обох пробірках. Речовина X — це
- А калій нітрат
- Б магній хлорид
- В амоній хлорид
- Г барій нітрат
15. Формули йонів, що зумовлюють постійну жорсткість води, наведено в рядку
- А Са2+, Mg2+, НСО-3
- Б Са2+, Mg2+, SO2-4
- В Na+, К+, НСО-3
- Г Na2+, К+, SO2-4
16. Укажіть правильне твердження
- А Чистий алюміній оксид — це мінерал алмаз
- Б Густина алюмінію більша, ніж густину заліза
- В У йона Аl3+ така сама електронна конфігурація, як і в атома Аргону
- Г У хімічних реакціях атоми Алюмінію віддають електрони й окиснюються
17. Для порівняння активності трьох металів, умовно позначеними літерами, і, провели дослідження (див. рисунок). Результати показали, що активність цих металів зростає в ряду
![]()
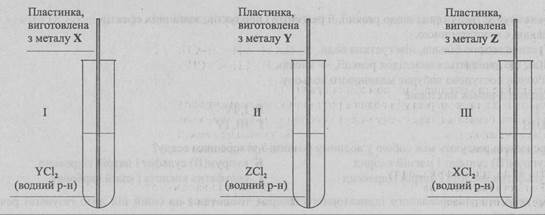
Проаналізуйте твердження.
I. З-поміж катіонів Х2+, Y2+, Z2+ найсильнішим є катіон Х2+.
II. Під час дослідження лише в пробірці III відбулася хімічна реакція.
Чи є з-поміж них правильні ?
- А правильне лише І
- Б правильне лише II
- В обидва правильні
- Г немає правильних
18. Укажіть речовини X та у схемі перетворень
![]()
|
X |
Y |
|
|
А |
Zn |
HCl |
|
Б |
Ni |
HCl |
|
В |
Zn |
Cl2 |
|
Г |
Ni |
Сl2 |
19. У ряду хімічних елементів
![]()
- А зростає електронегативність
- Б зростає число енергетичних рівнів в атомах
- В посилюються окисні властивості відповідних простих речовин
- Г посилюються неметалічні властивості відповідних простих речовин
20. Яку речовину потрібно використати, щоб продемонструвати отримання кисню термічним розкладанням солі?
- А калій гідрогенкарбонат
- Б кальцій силікат
- В кальцій карбонат
- Г калій нітрат
21. Середня сіль утвориться внаслідок реакції між речовинами X та Y, узятими в таких кількостях
|
Кількість речовини X, моль |
Формула речовини X |
Кількість речовини Y, моль |
Формула речовини Y |
|
|
A |
1 |
Н3РО4 |
1 |
NaOH |
|
Б |
1 |
Н3РО4 |
2 |
NaOH |
|
В |
1 |
H2SO4 |
1 |
KOH |
|
Г |
1 |
H2SO4 |
2 |
KOH |
22. Відрізнити пропан від карбон(ІV) оксиду можна за допомогою
- А бромної води
- Б вапняної води
- В розчину фенолфталеїну
- Г розчину калій перманганату
23. Укажіть назву за номенклатурою IUPAC речовини, структурна формула якої
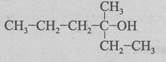
- А 2-пропілбутан-2-ол
- Б 2-етилпентан-2-ол
- В 3-метилгексан-3-ол
- Г 4-метилгексан-4-ол
24. Каталітична дегідрогенізація 2-метилпропану належить до реакцій
- А заміщення
- Б приєднання
- В ізомеризації
- Г відщеплення
25. Назви гомологів наведено в рядку
- А бут-1-ен і метилпроп-1-ен
- Б пент-1-ен і циклопентан
- В пент-1-ен і бут-1-ен
- Г бут-1-і бут-2-ен
26. Формулу речовини, яка реагує як із бромною водою, так і з амоніачним розчином аргентум(І) оксиду, наведено в рядку
- А СН3-С≡С-СН3
- Б СН3-СН=СН-СН3
- В СН2=СН-СН=СН2
- Г СН3-СН2-С≡СН
27. Проаналізуйте твердження. Чи є поміж них правильні?
I. Як бензен, так і гексан реагує з водним розчином калій перманганату.
II. Відрізнити бензен від генс-1-ену можна за допомогою бромної води.
- А правильне лише І
- Б правильне лише II
- В обидва правильні
- Г немає правильних
28. Укажіть назву третинного спирту
- А 2,3-диметилпентан-2-ол
- Б 2,2-диметилпентан-3-ол
- В 2-метилпентан-1-ол
- Г 3-метилпентан-2-ол
29. У пробірці до розчину Речовина X — це
- А етанол
- Б пропаналь
- В пропан-2-ол
- Г етан-1,2-діол
30. Укажіть рядок, де записано формули речовин, що вступають в реакцію, одним з продуктів якої є фенол

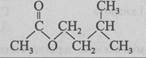
31. Унаслідок кислотного гідролізу речовини, структурну формулу якої наведено, утворюється
- А етанова кислота й 3-метилбутан-1-ол
- Б 3-метилбутанова кислота й етанол
- В етанова кислота й пентан-1-ол
- Г пентанова кислота й етанол
32. До моносахаридів належать
- А сахароза і фруктоза
- Б глюкоза і фруктоза
- В глюкоза і целюлоза
- Г сахароза і крохмаль
33. Правильне твердження щодо аніліну наведено в рядку
- А належить до ароматичних амінів вторинної будови
- Б змінює забарвлення універсального індикатора
- В на відміну від бензену реагує з бромною водою
- Г є сильнішою органічною основою, ніж діетиламін
34. Проаналізуйте твердження.
I. Каталітичною гідрогенізацією етину можна отримати етен.
II. З розчином калій перманганату реагує і етен, і етин.
III. Етен, на відміну від етену, знебарвлює бромну воду.
IV. Продуктом гідратації і етену, і етину є етанол.
Правильні з-поміж них лише
- А I, II
- Б I, IV
- В II, III
- Г III, IV
35. Укажіть формулу речовини X у схемі перетворень
![]()

36. Проаналізуйте твердження щодо речовини, структурні формули яких наведено.

I. Речовина 1 виявляє сильніші кислотні властивості, ніж речовина 2.
II. Речовина 2 належить до ненасичених одноатомних спиртів.
III. Речовини 2 і 3 взаємодіють з розчином натрій гідроксиду.
IV. У речовин 3 і 4 однаковий хімічний склад, але різна будова.
V. Речовини 3 і 4 належать до одного класу органічних сполук. Правильні з-поміж них лише
- А I, II
- Б II, III
- В III, IV
- Г IV, V
У завданнях 37-42 до кожного з чотирьох рядків інформації, позначених цифрами (ліворуч) виберіть один правильний, позначений буквою.
37. Установіть відповідність між схемою процесу відновлення та числом електронів, що беруть участь у ньому.
Схема процесу відновлення
- 1 ВrО-4 → ВrО-3
- 2 SO2-4 → H2S
- 3 ClO-3 → Cl-
- 4 NO-3 → NO
Число електронів
- А 2
- Б 3
- В 4
- Г 6
- Д 8
38. Установіть відповідність між реагентами та продуктами хімічної реакції.
Реагенти
- 1 метал і неметал
- 2 метал і кислота
- 3 амфотерний оксид і луг
- 4 амфотерний гідроксид і кислота
Продукти хімічної реакції
- A Na2ZnO2 і Н2O
- Б ZnCl2 і Н2О
- В ZnCl2 і Н2
- Г Na2ZnO2
- Д ZnCl2
39. Установіть відповідність між схемою перетворення та типом хімічної реакції.
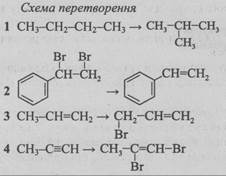
Тип хімічної реакції
- А заміщення
- Б приєднання
- В ізомеризації
- Г відщеплення
- Д повне окиснення
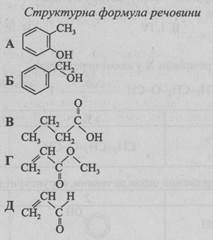
40. Установіть відповідність між класом органічних сполук і структурною формулою речовини, яка до нього належить.
Клас органічних сполук
- 1 карбонові кислоти
- 2 альдегіди
- 3 спирти
- 4 естери
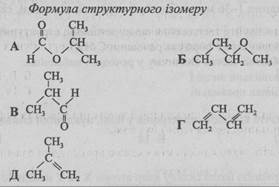
41. Установіть відповідність між назвою речовини та формулою одного з її структурних ізомерів.
Назва речовини
- 1 бутанова кислота
- 2 бутан-2-ол
- 3 бутаналь
- 4 бут-2-ен
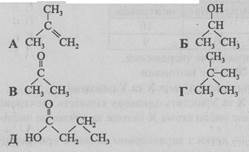
42. Установіть відповідність між хімічною реакцією та одним з її продуктів.
- 1 ізомеризація пентану
- 2 дегідрогенізація 2-метилпропану
- 3 часткове окиснення бутаналю
- 4 лужний гідроліз 2-бромопропану
Виконайте завдання 43-52.
43. Обчисліть масу (г) магній карбонату кількістю речовини 2,5 моль.
44. Газувата суміш складається з кисню й азоту в об’ємному співвідношенні 3 : 1. Обчисліть середню молярну масу (г/моль) цієї суміші.
45. Розбавлені розчини кислот добувають змішуванням концентрованих їхніх розчинів і води. Обчисліть масу (г) розчину з масовою часткою сульфатної кислоти 70 %, необхідного для приготування розчину масою 350 г з масовою часткою кислоти 12 %.
46. До розчину масою 90 г з масовою часткою літій гідроксиду 5 % добавили літій оксид кількістю речовини 0,1 моль. Обчисліть масову частку (%) лугу в розчині, що утворився.
47. Суміш, об’єм якої 5,6 л (н. у.), що складається з етану й етанаміну, пропустили крізь склянку із бромідною кислотою, взятою у надлишку. Унаслідок цього маса склянки збільшилась на 4,5 г. Обчисліть об’ємну частку етанаміну (%) у суміші реагентів.
48. Продукти повного окиснення 0,05 моль вуглеводню — карбон(ІV) оксид і вода. Їх послідовно пропустили крізь дві склянки: першу — з фосфор(V) оксидом, другу — з концентрованим розчином лугу. Унаслідок повного поглинання продуктів окиснення вуглеводню маси склянок збільшились: першої — на 3,6 г, другої — на 8,8 г. Укажіть молекулярну формулу вуглеводню. У відповіді запишіть число, що дорівнює сумі індексів у виведеній формулі.
49. Крізь вапняну воду, що містить 14,8 г кальцій гідроксиду пропустили 0,25 моль карбон(ІV) оксиду. Обчисліть масу середньої солі (г), що утворилась.
50. У кисні повністю спалили 5 г кам’яного вугілля. Унаслідок цього утворилось 8,96 л карбон(ІV) оксиду (н. у.). Обчисліть масову частку Карбону (%) у зразку вугілля.
51. Перетворіть схему реакції
KMnO4 + SO2 + Н2О → MnSO4 + K2SO4 + H2SO4
на хімічне рівняння, використавши метод електронного балансу. Укажіть коефіцієнт перед формулою відновника.
52. На повне відновлення міді із 40 г суміші, яка складається з оксидів Купруму (І) і Купруму (II), витратили 0,3 моль водню. Обчисліть масову частку купрум(І) оксиду (%) в суміші.
