Хімія. Повторне видання. 8 клас. Ярошенко (2025)
Тема 2. Досліджуємо гази довкілля

• Поняття молярного об’єму газу
• Закон Авогадро та його значення
• Показники нормальних умов
• Обчислення молярного об’єму газів
• Склад, властивості та застосування повітря
• Дослідження складу і властивостей повітря
• Відносна густина газів: тлумачення та обчислення
• Кисень і його властивості
• Добування і збирання кисню
• Формулювання і використання закону об’ємних відношень газів
• Роль кисню у природі та значення для людини
• Користь і шкода горіння
• Поняття про оксиди
• Поширення у природі та застосування озону і водню
• Ознайомлення з газоподібними сполуками Карбону — чадним і вуглекислим газами, метаном
• Діагностування й самооцінювання власних результатів навчання
§ 12. Молярний об'єм газів. Закон Авогадро
• Ілюструй малюнком твердий, рідкий та газоподібний агрегатні стани речовин і вислови судження про те, в якому агрегатному стані за однакових умов 1 моль речовини матиме найбільший об’єм.
• Чому шматочок льоду плаває у воді, а металева монета тоне в ній?
Опрацюй. Зрозумій. Використай
Тобі відома фізична величина — об’єм (V). Вона характеризує властивість тіл займати певну частину простору. Основна одиниця вимірювання об’єму — 1 м3.
Завдання 1. Пригадай і назви інші одиниці об’єму та співвідношення між ними.
Особливість газів полягає в тому, що, на відміну від рідин чи твердих тіл, вони здатні вільно поширюватися в усьому доступному для них просторі й рівномірно заповнювати його. Ось чому гази зберігають у закритих посудинах (мал. 8).

Мал. 8. Балони для зберігання газів
Тобі доводилося вимірювати об’єми твердих тіл правильної і неправильної форми, ти умієш виміряти об’єм рідини за допомогою мірного посуду.
У цьому параграфі ти дізнаєшся про молярний об’єм газів, знання якого дає змогу вимірювати / обчислювати об’єми газуватих речовин.
На малюнку 9 зображено 2 склянки. Одна з них наповнена водою кількістю речовини 1 моль, а друга — такою самою кількістю сульфатної кислоти.
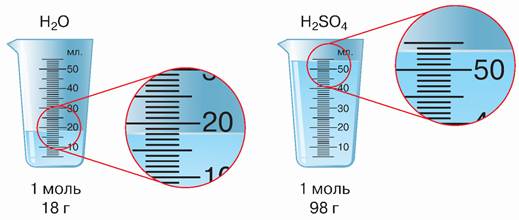
Мал. 9. Порівняння об’ємів води і сульфатної кислоти кількістю речовини 1 моль
Завдання 2. Однакові чи різні маса й об’єм води і сульфатної кислоти кількістю речовини 1 моль?
Можна продовжити розглядати інші приклади рідин кількістю речовини 1 моль, але всі вони будуть мати різні об’єми. Чи справджується цей факт щодо газів? Для відповіді на це запитання потрібно розглянути поняття «молярний об’єм газів».
МОЛЯРНИЙ ОБ’ЄМ ГАЗІВ (Vm). У наукових дослідженнях газуватих речовин та математичних обчисленнях часто користуються поняттям молярний об’єм газів, позначається Vm, читається: «ве-ем».
Молярний об’єм — об’єм, який займає газувата речовина кількістю речовини 1 моль за нормальних умов.
Температуру 0 °С і тиск 100,0 кПа називають нормальними умовами.
Нормальні умови скорочено позначають у круглих дужках першими малими літерами з крапкою після кожної — (н. у.). Молярний об’єм вимірюється в одиницях: метр кубічний на моль (м3/моль), дециметр кубічний на моль (дм3/моль) або літр на моль (л/моль).
Зазначимо, що тиск і температура суттєво впливають на об’єм газів, і ти про це дізнаєшся на уроках фізики.
Формулюємо навчальну проблему та розв’язуємо її
Як обчислити молярний об’єм газу?
Ти вже мав / мала справу з фізичною величиною «густина речовини (ρ)». Формула, за якою її обчислюють, передбачає наявність відомостей про масу та об’єм речовини. Вона записується так:
![]()
Виведемо похідну формулу для обчислення об’єму:
![]()
Якщо йдеться про молярний об’єм, то необхідно молярну масу газу поділити на його густину за нормальних умов (її можна дізнатись з інформаційних джерел):

Приклад 1. Обчислимо об’єм (в літрах) кисню кількістю речовини 1 моль за нормальних умов та кількість молекул у ньому. Густина кисню за нормальних умов — 1,43 г/л.

Візуалізуємо наведену інформацію у вигляді куба (мал. 10).

Мал. 10. Маса, об’єм, кількість молекул в одному молі кисню
ПЛІЧ-О-ПЛІЧ
Завдання 1. Обчисліть об’єм водню (ρ = 0,09 г/л), метану (ρ = 0,66 г/л), азоту (ρ = 1,25 г/л), вуглекислого газу (ρ = 1,98 г/л) кількістю речовини 1 моль за нормальних умов. Для кожної речовини зазначте кількість молекул в одному молі.
Роботу організуйте так: кожен член групи проводить обчислення для однієї з речовин. Отримані результати порівняйте і сформулюйте висновок про те, однаковими чи різними виявились об’єми газів та кількість структурних частинок (молекул), обчислених для кожної речовини членами вашої групи. Обміняйтеся результатами з іншим групами.
Завдання 2. Візуалізуйте одержані результати за зразком малюнка 10.
Завдання 3. Сформулюйте висновок щодо молярного об’єму газів (н. у.) та кількості молекул в одному молі газу.
Молярний об’єм газуватих речовин за нормальних умов приблизно однаковий і дорівнює 22,4 л/моль.
ЗАКОН АВОГАДРО. На початку XIX століття Амедео Авогадро висунув гіпотезу: якщо однакові об’єми газів перебувають в однакових умовах, то вони містять однакову кількість молекул. Спочатку цю гіпотезу інші вчені відхилили. І тільки після її експериментального підтвердження був сформульований закон, названий на честь його відкривача законом Авогадро.
Закон Авогадро: в однакових об’ємах різних газів за однакових умов (температури й тиску) міститься однакова кількість молекул. За нормальних умов вона дорівнює 6,02 • 1023 молекул.
Завдання 3. Чи відповідає закону Авогадро висновок за результатами виконаної вами групової роботи про кількість молекул у водні, метані, азоті, вуглекислому газі кількістю речовини 1 моль?
Відтепер ти знаєш, що за нормальних умов 1 моль будь-якого газу займає об’єм 22,4 л і містить 6,02 • 1023 молекул.
Використовуючи молярний об’єм газів, можна обчислити кількість речовини у певному об’ємі газу (н. у.). Обчислення проводять за формулою

Приклад 2. Обчислимо кількість речовини фтору, що займає об’єм 448 л за нормальних умов.

Приклад 3. Який об’єм займає карбон(ІІ) оксид кількістю речовини 4 моль за нормальних умов?

Завдання 4. Поміркуй, чи залежить об’єм певної кількості речовини від її молярної маси. Для підтвердження свого міркування порівняй молярні маси карбон(ІV) оксиду й нітроген(ІІ) оксиду та об’єм кожного газу кількістю речовини 4 моль (н. у.).
Формулюємо навчальну проблему та розв’язуємо її
Як обчислити об'єм за нормальних умов будь-якої газуватої речовини та кількість молекул у ній?

Приклад 4. Обчислимо об’єм за нормальних умов та кількість молекул у фторі F2 масою 7,6 г.

ТОБІ ДО СНАГИ
1. Який об’єм займає 1 моль газу за нормальних умов?
2. Як обчислити об’єм газуватої речовини за нормальних умов, якщо відома її маса або кількість речовини?
3. Який об’єм займає хлор масою 355 г (н. у.)?
4. Однаковий чи різний об’єм за нормальних умов займають 12,04 • 1023 молекул амоніаку і 68 г гідроген сульфіду H2S?
5. Увідповідни масу газу та його об’єм за нормальних умов.
Маса газу
- 1 3,4 г H2S
- 2 12,8 г SO2
- 3 36,5 г НСl
- 4 43,5 г Сl2О
Об’єм газу (н. у.)
- А 1,12 л
- Б 2,24 л
- В 4,48 л
- Г 11,2 л
- Д 22,4 л
6. Обери правильне твердження та обґрунтуй свій вибір.
Твердження 1. За нормальних умов метан масою 32 г і кисень масою 32 г мають однаковий об’єм.
Твердження 2. За нормальних умов азот масою 28 г займає вдвічі менший об’єм, ніж бутен масою 56 г, молекула якого складається з чотирьох атомів Карбону і восьми атомів Гідрогену.
