Хімія. Повторне видання. 8 клас. Ярошенко (2025)
§ 11. Діагностування результатів вивчення теми 1 «Пізнаємо кількісні закони хімії»
Параграф допоможе тобі повторити та узагальнити вивчені в темі 1 кількісні закони хімії й діагностувати результати навчання під час виконання вправ та онлайн-тесту.
Виконай вправи
1. Вибери формули бінарних сполук: ZnO, HNO3, О2, NaH, Не, Cu2O, CaSO4, СН4, С. Укажи валентність елементів у кожній з них.
2. Визнач правильно складені формули і виправ помилки в неправильно складених формулах: SO2, Fe3O2, СаО2, СН4, Na2O, АlO, Мg2О2.
3. Установи найлегший і найважчий серед наведених хімічних елементів: Fe, N, S, Са, О, Не.
4. Обчисли, яка сполука має більшу відносну молекулярну масу: бутан С4Н10 чи алюміній хлорид АlСl3.
5. Обчисли масову частку Нітрогену в нітратній кислоті HNO3.
6. Розташуй формули речовин CaS, CaO, CaSO4 за зростанням масової частки металічного елемента.
7. Яку масу має 1 моль водню, 2 моль глюкози С6Н12О6, 3 моль кальцій сульфіду CaS?
8. На малюнку зображено порції трьох речовин і зазначено їхні маси. Для кожної порції речовини обчисли: а) кількість речовини, б) кількість структурних частинок.

9. Заповни в зошиті таблицю 14.
Таблиця 14
|
Запис у рівнянні реакції |
Відносна молекулярна маса речовини |
Кількість речовини |
Маса зазначеної кількості речовини |
Масова частка Оксигену в речовині |
|
3H2SO4 |
||||
|
7О2 |
||||
|
5HNO3 |
||||
|
4С3Н8О3 |
||||
|
2Н3РО4 |
10. Обчисли масу сульфур(ІV) оксиду, який реагує з 11 моль води за схемою реакції SO2 + Н2О → H2SO3.
11. Нижче зображено 3D-модель хімічної реакції.
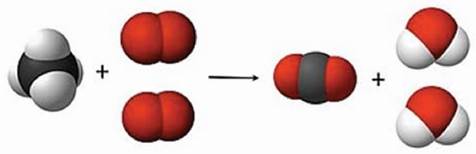
Умовні позначення атомів:
![]()
1. За моделлю ідентифікуй формули реагентів / реактантів і продуктів реакції.
2. Склади рівняння змодельованої реакції та обчисли:
- а) масу кисню, необхідну для утворення 4 моль вуглекислого газу;
- б) кількість речовини кисню, що взаємодіє з другим реагентом масою 64 г.
Виконай онлайн-тест.
Для цього перейди за покликанням qr.orioncentr.com.ua/XiPxW або скористайся смартфоном — зчитай QR-код.

Якщо результат виконання тесту тебе не задовольнить, тобі до снаги його покращити. Знайди можливість самостійно виправити зроблені помилки, щоб уникнути їх у майбутньому.
Бажаємо успіху та високого результату!
