Хімія. Повторне видання. 9 клас. Савчин
Цей підручник можна завантажити у PDF форматі на сайті тут.
§ 30. Вищі карбонові кислоти
Вивчивши матеріал параграфа, ви зможете:
- називати вищі карбонові кислоти, зокрема пальмітинову, стеаринову й олеїнову;
- пояснювати склад молекул стеаринової та олеїнової кислот; реакції добування мила;
- характеризувати властивості мила, його склад, мийну дію;
- обґрунтовувати застосування жирів, їх біологічну дію;
- висловлювати судження про значення вищих карбонових кислот.
Поняття про вищі карбонові кислоти. На відміну від етанової кислоти, молекули вищих карбонових кислот містять у своєму складі понад 10 атомів Карбону. Вони належать до одноосновних, бо в кожній молекулі наявна тільки одна карбоксильна група. Серед вищих карбонових кислот є кислоти насиченого й ненасиченого складу.
До вищих насичених одноосновних карбонових кислот належать пальмітинова (гексадеканова) і стеаринова (октадеканова) кислоти.
Розглянемо склад їхніх молекул. Хімічна формула пальмітинової кислоти СН3—(СН2)14—СООН. Її молекула містить насичений вуглеводневий замісник —С15Н31 і карбоксильну групу —СООН.
Хімічна формула стеаринової кислоти СН3—(СН2)16—СООН. Вуглеводневий замісник —С17Н35 сполучений із карбоксильною групою.
З вищих ненасичених карбонових кислот поширена олеїнова (октадек-9- енова) кислота, молекулярна формула якої С17Н33—СООН. Масштабні моделі молекул пальмітинової та олеїнової кислот зображено на рисунках 103 і 104.

Рис. 103. Масштабна модель молекули пальмітинової кислоти
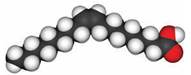
Рис. 104. Масштабна модель молекули олеїнової кислоти
Фізичні властивості вищих карбонових кислот. Пальмітинова й стеаринова кислоти — тверді речовини білого кольору (рис. 105), нерозчинні у воді. Вони не мають запаху, масні на дотик. Упевнитися в цьому можна, дослідивши стеаринову свічку.

Рис. 105. Стеарин
Вищі ненасичені кислоти здебільшого рослинного походження, хоча є винятки. Олеїнова кислота — рідина, жирна, нерозчинна у воді.
Хімічні властивості. Вищі карбонові кислоти, насичені й ненасичені, реагують із розчинами лугів з утворенням солей пальмітинової, стеаринової та олеїнової кислот. Рівняння реакцій:
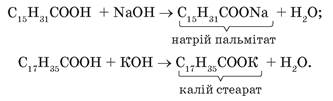
Унаслідок взаємодії з натрій та калій гідроксидами утворюються натрієві й калієві солі пальмітинової та стеаринової кислот, які є основною складовою частиною мила.
Пальмітинова й стеаринова кислоти реагують із солями в розчинах. Наприклад:
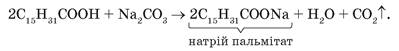
Олеїнова кислота, реагуючи з лугами, утворює солі — олеїноати.
• Складіть самостійно рівняння реакцій взаємодії олеїнової кислоти з натрій гідроксидом і натрій карбонатом.
Взаємодія вищих карбонових кислот із содою — це промисловий спосіб виробництва господарського мила. Додаючи ароматизатори, барвники, жири, рослинні добавки, парфуми, з нього виготовляють різні сорти туалетного мила. Його якість залежить від інгредієнтів і способу виробництва.
Мийна дія мила. Основною речовиною мила є солі вищих карбонових кислот. Їх структурні одиниці містять неполярний великий (С15-С17) вуглеводневий замісник і полярну складову — групу атомів -COO-Na+ або -COO-К+.
Потрапляючи у воду, йони кислотних залишків вищих карбонових кислот своїми полярними полюсами орієнтуються до полярних молекул води, а неполярними вуглеводневими замісниками — до неполярних частинок бруду. Частинки бруду, потрапляючи в оточення «мильних» йонів, легко відщеплюються та поширюються між молекулами води.
Нерозчинними у воді є солі вищих карбонових кислот, у складі яких є йони Кальцію та Магнію. Вони утворюються внаслідок реакцій обміну між солями, що містяться у твердій воді й випадають в осад. Унаслідок цього мило втрачає мийну властивість.
Останнім часом став поширеним спосіб миловаріння в домашніх умовах. Популярність такого мила зумовлена тим, що воно якісне й корисне. Для виготовлення мила в домашніх умовах використовують натуральні жири — як тверді, так і рідкі. Це, зокрема, свиняче, яловиче й бараняче сало, оливкова, лляна, конопляна, пальмова й інші олії, натуральні барвники та запашні трави, фрукти. Шматочком мила надають різні форму й колір, для привабливішого вигляду (рис. 106).

Рис 106. Мило, виготовлене в домашніх умовах
Фізіологічна дія мила. Насамперед мило є засобом гігієни людини.
Туалетне мило виявляє корисну дію залежно від інгредієнтів у ньому. Це можуть бути екстракти різних трав, зокрема ромашки, алое, нагідки лікарської (календули), звіробою, ялиці.
Важливо вміти правильно добирати мило для власних потреб. У цьому вам допоможе вміння прочитати та проаналізувати етикетку. Надмірна кількість синтетичних речовин, ароматизаторів, барвників, речовин для дезінфікації негативно впливає на шкіру, робить її сухою та грубою, спричиняє алергічні прояви.
У кожному господарстві мило є засобом дотримання чистоти не тільки рук і тіла, а й одягу (прання), посуду, поверхонь меблів.
У природі трапляються рослини, що містять сапоніни. Назва походить від латинського слова sapo, що означає «мило». Сапоніни містяться в різних частинах рослин: коренях і кореневищах, стеблах, листках, квітах. Їм властива висока поверхнева активність. Сапоніни є в бузині, кореневищах мильнянки лікарської, папороті-орляка, коренях женьшеню, синюхи блакитної, калюжниці болотної, білої лілії та інших.
ПІДСУМОВУЄМО ВИВЧЕНЕ
• Вищі одноосновні карбонові кислоти поділяють на насичені й ненасичені. З насичених найбільш поширені пальмітинова та стеаринова кислоти, з ненасичених — олеїнова.
• Молекули вищих карбонових кислот містять неполярні вуглеводневі замісники з великою кількістю атомів Карбону (С15-С17) і полярні карбоксильні групи -СООН.
• Натрієві й калієві солі вищих карбонових кислот називають милами. Натрієві солі утворюють тверде мило, калієві — рідке.
• Мийна дія мила зумовлена його складом і будовою.
• Мило — засіб гігієни, запорука чистоти посуду, одягу, поверхонь меблів.
• Мийна дія властива багатьом рослинам, що містять сапоніни.
ЗАВДАННЯ ДЛЯ САМОКОНТРОЛЮ
1. Укажіть молекулярну формулу пальмітинової кислоти.
- А С17Н35-СООН
- Б С15Н31-ОН
- В С15Н31-СООН
- Г С17Н33-СООН
2. Укажіть скорочену структурну формулу олеїнової кислоти.
- А СН3-(СН2)4-СН2-(СН2)4-СООН
- Б СН3-(СН2)7-СН2-(СН2)7-СООН
- В СН3-(СН2)5-СН2-(СН2)5-СООН
- Г СН3-(СН2)7-СН=СН-(СН2)7-СООН
3. Укажіть реакцію утворення натрій стеарату.
- А 2С15Н31-СООН + Na2CО3 → 2C15H31-COONa + Н2О + СО2↑
- Б 2С17Н35-СООН + К2СО3 → 2С17Н31-СООК + Н2О + СО2↑
- В 2С17Н35-СООН + Na2CO3 → 2С17Н35-COONa + Н2О + CO2↑
- Г С15Н31-СООН + NaOH → C15H31-COONa + Н2О
4. Порівняйте склад і фізичні властивості стеаринової та олеїнової кислот. Складіть скорочені структурні формули.
5. Обчисліть масову частку Карбону в складі калій пальмітату.
6. Обчисліть масу натрій стеариноату, що утворився внаслідок повної взаємодії натрій карбонату масою 318 кг із відповідною кислотою. Якій кількості речовини відповідає маса утвореного продукту реакції?
7. Унаслідок взаємодії олеїнової кислоти з калій гідроксидом утворилася сіль масою 64 кг. Обчисліть маси реагентів. Назвіть утворену сіль.
ЦІКАВО ЗНАТИ
• Новий винахід британських учених стосується так званого «магнітного мила». У ньому містяться солі Феруму. Таке мило розчиняє бруд, який потім можна зібрати за допомогою магніту, що й зумовило його назву. Цей винахід має важливе значення, оскільки його можна застосовувати для очищення води стічних труб, а також водойм після катастроф, пов’язаних із розтіканням нафти.
Дж. Істоу, професор хімії Брістольського університету, повідомив, що «магнітне мило» зможе відчистити від нафти пір’я птахів.
ДОМАШНІЙ ЕКСПЕРИМЕНТ
Порівняння мийної дії мила та прального порошку вітчизняного виробника
1. Приготуйте розчини мила та прального порошку однакових об’ємів по 4 порції кожного.
2. Наберіть у склянки воду з різних джерел: водопровідну, джерельну, мінеральну, річкову об’ємом по 50 мл.
3. До склянок із водою з різних джерел додайте почергово: а) розчин мила; б) розчин прального порошку. Струсіть вміст склянок. Зробіть висновок про мийну дію мила та порошку за інтенсивністю утвореної піни.
НАВЧАЛЬНИЙ ПРОЄКТ
І. Виконайте навчальний проєкт із теми «Виготовлення мила з мильної основи».
II. Презентуйте проєкту класі. Обговоріть його з однокласниками й однокласницями.
