Хімія. Рівень стандарту. 11 клас. Савчин
Цей підручник можна завантажити у PDF форматі на сайті тут.
§ 20. ОКСИДИ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ, ЇХНІЙ ВМІСТ В АТМОСФЕРІ
Опанувавши матеріал параграфа, ви зможете:
- називати оксиди неметалічних елементів;
- складати рівняння реакцій, які характеризують хімічні властивості й одержання кислотних оксидів;
- характеризувати фізичні й хімічні властивості оксидів неметалічних елементів; застосування оксидів неметалічних елементів;
- пояснювати антропогенні та природні причини появи в атмосфері оксидів неметалічних елементів;
- висловлювати судження щодо екологічних наслідків викидів в атмосферу оксидів Карбону, Нітрогену й Сульфуру; кислотних дощів, парникового ефекту.
Оксиди неметалічних елементів. Неметалічні елементи утворюють з Оксигеном бінарні сполуки — оксиди неметалічних елементів, або кислотні оксиди. Найважливіші з них — оксиди Карбону, Силіцію, Нітрогену, Фосфору, Сульфуру та Хлору. За нормальних умов вони перебувають у різних агрегатних станах: твердому, рідкому або газоподібному (табл. 10).
Таблиця 10
Агрегатний стан оксидів неметалічних елементів
|
Агрегатний стан |
Назви оксидів за систематичною номенклатурою |
Формули |
|
Газоподібний |
Карбон(ІІ) і карбон(IV) оксиди |
СО, СО2 |
|
Сульфур(IV) оксид, нітроген(IV) оксид |
SO2, NO2 |
|
|
Твердий |
Силіцій(IV) оксид, фосфор(V) оксид, нітроген(V) оксид |
SiO2, P2O5, N2O5 |
|
Рідкий |
Гідроген оксид, сульфур(VI) оксид |
Н2О, SO3 |
Фізичні властивості. Оксиди неметалічних елементів — це молекулярні сполуки з молекулярними кристалічними ґратками (крім SiO2, що має атомні кристалічні ґратки). Від структури й залежать їхні властивості. Оксиди молекулярної будови — гази, без запаху (СО, NO, СО2) або з різким запахом (SO2, NO2). Карбон(IV) і сульфур(IV) оксиди за певних температур переходять в інший агрегатний стан: перший утворює тверду речовину (сухий лід), другий — безбарвну рідину, яку зберігають у сталевих цистернах. Випаровуючись, обидва оксиди спричиняють охолодження.
Нітроген з Оксигеном утворює п'ять оксидів. Докладнішу інформацію про їхні назви, молекулярні формули та фізичні властивості ви дізнаєтеся, розглянувши рис. 37.

Рис. 37. Схема класифікації оксидів Нітрогену
Силіцій(IV) оксид — тверда кристалічна речовина. Його температура плавлення дуже висока — 1728 °С порівняно з карбон(IV) оксидом, температура плавлення якого становить 56,6 °С. Така відмінність зумовлена різною будовою кристалічних ґраток цих оксидів.
Фосфор(V) оксид — пухкий порошок, білого кольору, з густиною 2,3 г/см3, гігроскопічний (поглинає вологу), легкоплавкий, з різким запахом. Типовий кислотний оксид.
Хімічні властивості. Для кислотних оксидів характерні реакції взаємодії з водою, основними оксидами й лугами.
Взаємодія з водою. Щоб з'ясувати, як відбувається реакція взаємодії фосфор(V) оксиду з водою, проведемо декілька дослідів.
Дослід 1 (у витяжній шафі). У колбу, наповнену киснем, опустимо попередньо запалений червоний фосфор. Під час горіння утворюється фосфор(V) оксид, який наповнює колбу густим білим снігоподібним димом.
Доллємо до колби з фосфор(V) оксидом воду, колбу декілька разів струснемо. Утворюється прозорий розчин.
Дослід 2. До розчину, що утворився в колбі, доллємо розчин лакмусу.
Спрогнозуйте, що спостерігатимемо під час випробування розчину лакмусом.
Взаємодія з водою відбувається неоднаково й залежить від кількості води. Запишемо рівняння реакцій:

Однак не всі кислотні оксиди взаємодіють з водою. Нерозчинним у воді є силіцій(IV) оксид.
Взаємодія з основними оксидами. Якщо силіцій(IV) оксид нагріти з кальцій оксидом, то утворюється середня сіль — кальцій силікат. Рівняння реакції:
![]()
Взаємодія з лугами. Щоб з'ясувати, чи взаємодіють кислотні оксиди з лугами, проведемо дослід.
Дослід 3. Наллємо в хімічний стакан розчин натрій гідроксиду, підфарбований фенолфталеїном. Пропустимо крізь цей розчин карбон(ІV) оксид.
Спрогнозуйте, які зміни відбуватимуться в хімічному стакані.
Рівняння реакції: 2NaOH + CO2 = Na2CO3+ H2O.
Антропогенні та природні причини появи в атмосфері оксидів неметалічних елементів. Джерелами викидів в атмосферу оксидів неметалічних елементів є численні підприємства, які не мають потрібних очисних споруд, теплоелектростанції, транспортні засоби, населені пункти, неякісне технічне обладнання.
Унаслідок виробничих процесів різних галузей промисловості та сільського господарства відбуваються колосальні зміни в атмосфері планети. Промислові виробництва всієї Землі, автомобільний транспорт викидають в атмосферу величезні обсяги карбон(IV) оксиду (вуглекислого газу), сульфур(ІV) оксиду, гідроген сульфіду, нітроген(ІІ) і нітроген(IV) оксидів. Це призводить до зменшення товщини озонового шару, який захищає поверхню Землі від ультрафіолетового випромінювання, випадання кислотних дощів, виникнення парникового ефекту. Учені зазначають, що протягом останніх 30 років концентрація озону в атмосфері зменшилася в десятки разів. Це може бути причиною утворення чорних дір в атмосфері. Велика кількість вуглекислого газу в атмосфері зумовлює глобальне потепління на планеті.
З'ясуємо, які забруднювачі атмосфери спричиняють кислотні дощі. Насамперед це сульфур(ІV) оксид, що утворюється під час процесів горіння, зокрема нафти й мазуту, кам'яного вугілля; у металургії — під час випалювання та переробки сульфатних руд, виробництва сульфатної кислоти й кольорових металів; робота транспорту призводить до утворення сульфур(ІV) і карбон(ІV) оксидів.
В атмосфері сульфур(ІV) оксид окиснюється до сульфур(VІ) оксиду, а той під час випадання дощів перетворюється на сульфатну кислоту. Сульфур(VІ) оксид гігроскопічний, тобто має здатність поглинати вологу з повітря, утворюючи дрібні краплі сульфатної кислоти. Цей процес відображає такий ланцюг перетворень:
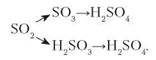
В атмосфері, подібно до оксидів Сульфуру, відбуваються перетворення оксидів Нітрогену на нітратну кислоту. Запишемо цей процес схемою:
N2 → NO → NO2 → HNO3.
Взаємодія нітроген(ІV) оксиду з водою може відбуватися з утворенням нітритної та нітратної кислот, а в надлишку кисню — тільки нітратної кислоти. Рівняння реакцій:
2NO2 + Н2О = HNO3 + HNO2; 4NO2 + 2Н2О + О2 = 4HNO3.
Природними причинами утворення в атмосфері оксидів неметалічних елементів є виверження вулканів, гниття органічних речовин.
Під час гниття органічних решток виділяється гідроген сульфід, що має здатність окиснюватися до сульфур(ІV) оксиду атмосферним киснем та озоном. Рівняння реакцій:
2H2S + 3О2 = 2SO2+ 2H2O; H2S + O3 = SO2 + Н2О.
Під час виверження вулканів в атмосферу потрапляє велика кількість карбон(ІV) і сульфур(ІV) оксидів.
Складіть самостійно рівняння реакцій утворення сульфатної та нітратної кислот, що відбуваються в атмосфері під час випадання дощів.
Після випадання кислотних дощів відбуваються зміни в природі: листя на деревах і кущах жовтіє, іноді покривається ржаво-бурим нальотом, з'являється неприємний прілий запах тощо. Це свідчить про те, що кислотні дощі знищують екосистеми, сповільнюють ріст культурних рослин, знижують їхню стійкість до грибкових захворювань, послаблюють протидію мікроорганізмам.
Кислотні дощі негативно діють на ґрунти, підвищуючи їхню кислотність, а отже, знижують урожайність.
Оксиди Сульфуру й Нітрогену є отруйними, тож негативно впливають на здоров'я людини. Наявність їх у повітрі спричиняє подразнення дихальних шляхів, виникнення бронхіту й інших хвороб, зниження імунітету, що призводить до зменшення тривалості життя людей.
Отже, щоб запобігти антропогенному впливу на забруднення атмосфери планети, потрібно усвідомити ті наслідки, які спричиняють небезпеку здоров'ю людей та всього живого, і дотримуватися відповідних правил, а саме: 1) зменшувати відсоток пального, яке призводить до викидів в атмосферу отруйних газів, переходячи на екологічно чисті види палива; 2) застосовувати очисні споруди на підприємствах, які викидають ці гази; 3) не спалювати суху траву, відходи деревини, пластик; 4) збільшувати площі зелених насаджень, які перетворюють карбон(IV) оксид на органічну речовину, очищаючи атмосферу та поповнюючи її киснем.
Застосування оксидів неметалічних елементів. Оксиди неметалічних елементів набули широкого застосування (табл. 11).
Таблиця 11
Застосування оксидів неметалічних елементів
|
Оксид |
Формула |
Застосування |
|
Карбон(IV) оксид |
СО2 |
У хімічній промисловості для добування солей карбонатної кислоти; для газування води, приготування газованих напоїв; як холодоагент для збереження м'ясних продуктів, риби, морозива, овочів та інших продуктів; під час виробництва вин і пива; у вогнегасниках; для прискорення достигання овочів у теплицях. Регулює тепловий баланс планети; бере участь у процесі фотосинтезу. |
|
Карбон(II) оксид |
СО |
Як паливо в суміші з воднем; для синтезу метанолу. |
|
Сульфур(IV) оксид |
SO2 |
Сировина для виробництва сульфатної кислоти та її солей; для знезараження зерно- й овочесховищ від шкідників і мікроорганізмів; відбілювання соломи, шовкових і вовняних тканин; дезінфекції ємкостей на винних і пивних заводах. |
|
Сульфур(VI) оксид |
SO3 |
Виробництво сульфатної кислоти та її солей; як водовідбірний засіб. |
|
Силіцій(IV) оксид |
SіО2 |
У будівельній справі для виробництва бетону, цегли, стекол, кераміки, шліфувальних матеріалів; у фармацевтиці як сорбент (аерогель, селікагель); для виробництва пористих матеріалів; в оптичній та парфумерній промисловостях; як теплоізолятор; кварц — у ювелірній справі, для виробництва кварцового термостійкого скла. |
|
Нітроген(ІV) оксид |
NO2 |
Як окисник у ракетному паливі; у виробництві нітратної кислоти, нітратів, мінеральних добрив. |
|
Фосфор(V) оксид |
Р2О5 |
Добування ортофосфатної кислоти; в органічному синтезі, для осушення газів. |
Фізіологічна дія. Багато оксидів неметалічних елементів проявляють токсичну дію на організм людини. Дуже отруйною речовиною є карбон(ІІ) оксид, або чадний газ. Його молекули сполучаються з гемоглобіном крові значно міцніше за молекули кисню, унаслідок чого припиняється перенесення кисню до клітин організму. Вуглекислий газ хоча й не токсичний, але за надмірної кількості в людини виникає задуха або зупинка дихання. Оксиди Сульфуру й Нітрогену уражають слизові оболонки дихальних шляхів, спричиняють опіки шкіри. Пари оксидів Нітрогену призводять до збільшення розмірів печінки й селезінки, розладу психіки.
ПІДСУМОВУЄМО ВИВЧЕНЕ
• Оксиди неметалічних елементів перебувають у трьох агрегатних станах. Це переважно речовини молекулярної будови. Атомні кристалічні ґратки властиві силіцій(IV) оксиду.
• Оксиди неметалічних елементів — це кислотні оксиди. Вони вступають у хімічну взаємодію з водою, основними оксидами й лугами.
• Поява в атмосфері оксидів неметалічних елементів зумовлена викидами численних підприємств, теплоелектростанцій, роботою транспортних засобів, функціонуванням населених пунктів, недоброякісним технічним обладнанням.
• Основними забруднювачами атмосфери є карбон(IV) оксид, сульфур(IV) і сульфур(VI) оксиди, нітроген(ІІ) і нітроген(IV) оксиди.
• Процес утворення кислотних дощів за участю сульфур(IV), нітроген(ІІ) і нітроген(IV) оксидів відбувається за такими ланцюгами перетворень:

• Кислотні дощі негативно впливають на рослинність, знижують родючість ґрунтів, а оксиди Сульфуру та Нітрогену спричиняють у людей захворювання органів дихання.
• Оксиди неметалічних елементів набули широкого застосування в господарстві України.
ЗАВДАННЯ ДЛЯ САМОКОНТРОЛЮ
- 1. Назвіть неметали, які набули широкого застосування в господарстві України.
- 2. Охарактеризуйте сфери застосування: а) водню; б) кисню та озону; в) сірки; г) фосфору; ґ) вуглецю.
- 3. Назвіть причини антропогенного та природного забруднення атмосфери оксидами неметалічних елементів.
- 4. Складіть рівняння реакцій, що відбуваються за схемами:
а) S → SO2 → SO3 → H2SO4 → Na2SO4 → BaSO4;
б) N2 → NO → NO2 → HNO3 → Ca(NO3)2.
- 5. Складіть рівняння реакцій між: а) азотом і киснем; б) фосфором і киснем; в) вуглецем і сіркою; г) воднем і сіркою. Складіть електронний баланс, укажіть окисник і відновник.
- 6. Під час грози атмосферний азот об'ємом 134,4 л (н. у.) перетворився на оксид, який сполучився з дощовою водою з утворенням кислоти. Обчисліть масу кислоти, що випала з дощем на землю.
- 7. Сульфур(IV) оксид масою 19,2 г окиснили та піддали дії води. Обчисліть масу й кількість речовини утвореного продукту. Назвіть утворену речовину.
