Природознавство. 11 клас. Ільченко
§ 22. Мила і синтетичні мийні засоби
Опанувавши матеріал параграфа, ви дізнаєтесь про склад і хімічну природу мил та інших мийних засобів, про причини їхньої мийної дії, необхідність збереження водойм від шкідливих викидів мийних засобів.
Значення мила і мийних засобів. Мило (мал. 3.30) та синтетичні мийні засоби широко використовуються у сучасному виробництві та побуті. Усі ми щодня використовуємо мило для особистої гігієни. Відомо, що на кожному квадратному сантиметрі шкіри людини одночасно знаходиться від 100 тис. до 1 млн. мікроорганізмів. Шкіра виділяє особливі захисні речовини, що руйнують білки бактерій. Однак при її забрудненні виділення цих речовин різко знижується. При митті значна частина мікробів зі шкіри видаляється. Тому потрібно слідкувати за чистотою шкіри й одягу.Наведи приклади використання мила та інших мийних засобів у побуті та на виробництві.

Мал. 3.30. Мило — поширений засіб особистої гігієни
Хімічна природа мила та синтетичних мийних засобів. Мило було відоме людині ще в стародавні часи. Миловарна промисловість існувала вже наприкінці епохи середньовіччя. Проте про хімічну сутність процесів добування мила та його мийної дії тоді майже нічого не знали. Лише в XIX ст. завдяки дослідженням багатьох учених, перш за все французьких хіміків Е. Шевреля та М. Бертло, була встановлена хімічна природа жирів і стала зрозумілою реакція їх омилення.
Мило за хімічним складом — це натрієва чи калієва сіль вищих карбонових кислот, наприклад, стеаринової: С17H35COONa, С17Н35COOK. Натрієві мила тверді, а калієві — рідкі.
У виробництві мило добувають шляхом гідролізу (омилення) жирів.
1. Згадай, які речовини називають естерами.
2. Що являють собою жири? Що відбувається при гідролізі (омиленні) жирів?
Ви вже знаєте, що за хімічною природою жири — це естери, утворені трьохатомним спиртом гліцеролом і вищими карбоновими кислотами — переважно пальмітиновою СН3(СН2)14СООН, стеариновою СН3(СН2)16СООН і олеїновою СН3(СН2)7СН = СН(СН2)7СООН. У рідких рослинних жирах переважають ненасичені кислоти, зокрема олеїнова, які містять подвійні зв’язки, а в твердих тваринних жирах — насичені кислоти (стеаринова, пальмітинова тощо), в складі яких подвійні зв’язки відсутні.
У лужному середовищі жири піддаються гідролізу, або омиленню, розкладаючись на гліцерин та солі карбонових кислот:
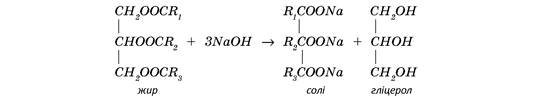
Оскільки жири розкладаються у лугах, то більшість мийних засобів мають лужне середовище.
Останнім часом з милом (або замість нього) все частіше використовують синтетичні мийні засоби (СМЗ). Їх виготовляють на основі натрієвих солей естерів сульфатної кислоти та вищих спиртів:
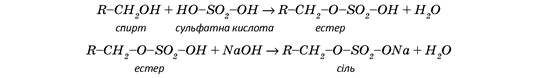
Молекули солей, що є основною складовою мил та СМЗ, являють собою ланцюги, які мають гідрофобну та гідрофільну частини. «Філео» у перекладі з грецької — люблю. Отже, гідрофільний — це той, що любить воду, взаємодіє з її молекулами. «Фобос» означає страх, боязкість. Отже, гідрофобний — це той, що боїться води, уникає її. Неполярна частина молекули солі — вуглеводневий замісник СН3-СН2-СН2-СН2-... є гідрофобною, а полярна частина, що містить, наприклад, карбоксильну групу - СООН, — гідрофільною. Молекули таких речовин здатні адсорбуватись, тому їх називають поверхнево-активними речовинами (ПАР).
Згадай, яке явище називають адсорбцією. Чому воно відбувається?
Як діють мийні засоби? Забруднення дуже різноманітні за своєю хімічною природою, проте найчастіше вони малорозчинні або зовсім нерозчинні у воді. Такі речовини, як правило, є гідрофобними, тобто з водою вони не взаємодіють (у таких випадках кажуть, що вони не змочуються водою). Для видалення таких забруднень із поверхні треба використовувати мийні засоби.
Гідрофобна частина молекули речовини, що виявляє мийну дію, взаємодіє з неполярними молекулами забруднення, а гідрофільна (полярна) частина цієї молекули взаємодіє з полярними молекулами води (мал. 3.31). Полярна група молекули ПАР намагається проникнути у водне середовище, «тягнучи» при цьому за собою частинки забруднювача, «приєднані» до гідрофобного кінця цієї молекули. Крім того, молекули ПАР проникають у мікроскопічні щілини між частинками бруду і поверхнею, яка очищується, що також сприяє відриванню частинок бруду від поверхні. Окремі частинки бруду утворюють у водному середовищі емульсії або суспензії, що стабілізуються молекулами ПАР.
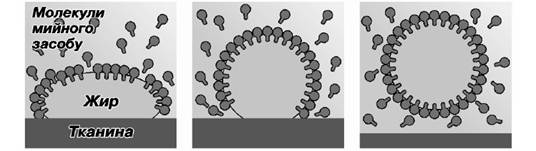
Мал. 3.31. Схема дії мийних засобів
Для покращення прання брудної білизни мийний розчин нагрівають (чому?) та використовують механічну дію. Більшість мийних засобів утворюють стійку піну, яка також покращує механічне видалення бруду.
Отже, будь-який мийний засіб виконує подвійну функцію — взаємодіє із забруднюючою речовиною, видаляючи її з поверхні, та переводить забруднення у водний розчин.
Використання мийних засобів у побуті. Найчастіше мийний засіб використовують для прання білизни. Однак нерідко при пранні мило втрачає свою мийну дію. Це трапляється у випадках, коли у воді, що використовується для прання, міститься велика кількість солей Кальцію та Магнію. Таку воду, як ви знаєте, називають твердою. Мило погано розчиняється у твердій воді, через те, що залишки вищих карбонових кислот утворюють із йонами Кальцію та Магнію нерозчинні солі:
2С17H35COONa + СаСl2 = (C17H35COO)2Са + 2NaCl
Щоб мило не втрачало своїх якостей у такій воді, останню «пом’якшують». Для цього часто використовують соду (чому?). На відміну від мила, більшість СМ3 не утворюють нерозчинних солей і тому не втрачають мийної дії у воді будь-якої твердості.
Сьогодні промисловість виробляє великий асортимент мил і мийних засобів. Для виготовлення туалетного мила до нього додають парфумерні віддушки, відбілювачі, барвники тощо. Як правило, мила та СМЗ утворюють лужне або слабколужне середовище. Існують і такі мийні засоби, що утворюють середовище, близьке до нейтрального. Для сухої та нейтральної шкіри краще використовувати мило з нейтральним середовищем, а для жирної — із слабколужним.
Важливою умовою широкого застосування синтетичних ПАР як мийних засобів у побуті та промисловості є можливість їхнього біологічного розкладу, наприклад, бактеріями. Ця обставина має велике значення з екологічної точки зору. Справа в тому, що синтетичні мийні засоби часто містять фосфати і до того ж не піддаються руйнуванню після їх використання. Потрапляючи у водойми (ставки, озера) вони створюють умови для сильного розростання зелених водних рослин. Це може призвести до загибелі флори і фауни водойм, оскільки водорості інтенсивно поглинають кисень, розчинений у воді. Ось чому перед хіміками стоїть важливе завдання створення таких мийних засобів, які б забезпечували не тільки високу мийну дію, але й руйнувалися під дією мікроорганізмів.
Лабораторний дослід 9. Порівняння властивостей мила і синтетичних мийних засобів
Вам необхідно дослідити ефективність мийної дії мила та прального порошку у звичайній та твердій воді.
Перевірте свою готовність до проведення досліджень.
1. Які бувають мила?
2. Назвіть спільні та відмінні риси у складі мила та синтетичних мийних засобів (СМЗ).
3. Поясніть мийну дію мила та СМЗ. Які переваги мають СМЗ над милом?
4. Чим зумовлена твердість води?
5. Наведіть правила безпеки при нагріванні речовин і безпечного поводження з лугами та кислотами.
6. Для розщеплення молекул жиру застосовують «каустичну соду». Йони кислотних залишків пальмітинової та стеаринової кислот, вступаючи в реакцію з каустичною содою, утворюють мило. Запишіть рівняння реакції в молекулярному та йонному вигляді.
7. Якщо до складу мила входять йони Калію, його використовують для виготовлення кремів та засобів для гоління. Чому? Запишіть йонне рівняння взаємодії пальмітинової кислоти з калій гідроксидом.
Реактиви і матеріали: Водний розчин мила (w(мила) = 1 %), водний розчин прального порошку (w(порошку) = 1 %), спиртовий розчин фенолфталеїну.
Дослід 1. Випробування розчинів мила та прального порошку на хімічний характер середовища. У дві пробірки налийте по 1-2 мл розчинів мила і прального порошку. Додайте декілька крапель фенолфталеїну до вмісту кожної пробірки. Якого забарвлення набули розчини? Запишіть ваші спостереження і зробіть висновки.
Дослід 2. Поводження мила і прального порошку у твердій воді. У дві пробірки налийте по 2-5 мл твердої води. У першу пробірку додайте краплями розчин мила, а в другу — розчин прального порошку. Після кожної краплі вміст пробірок збовтуйте. Що спостерігаєте? У якій пробірці утворюється стійка піна? Чому? Зробіть висновок. Запишіть рівняння хімічних реакцій у молекулярному та йонному вигляді.
Зробіть загальний висновок. Як зберегти водойми, які заболочуються внаслідок викидів мийних засобів разом із стічними водами?
Мийна дія мила та СМЗ зумовлена наявністю у їхньому складі поверхнево-активних речовин, які мають гідрофільну (полярну) та гідрофобну (неполярну) частини. Сучасна промисловість виробляє велику кількість мил та синтетичних мийних засобів, які широко використовуються у побуті та на виробництві.
Перевір себе
- 1. Що являють собою мила?
- 2. Який склад найпоширеніших синтетичних мийних засобів?
- 3. Що зумовлює мийну дію цих засобів?
- 4. Які чинники слід враховувати при виборі мийного засобу?
Поміркуй
1. Чи можна випрати білизну в морській воді за допомогою мила? Чому?
2. Чому СМЗ не втрачають своїх властивостей у твердій воді?
3. Щоб ти порадив(ла) використовувати для миття дуже жирного посуду — засіб із нейтральним середовищем чи лужним — і чому?
4. Мило піддається гідролізу гарячою водою:
C17H35СООNa + Н2О ⇄ С17H35CООН + NaOH
Для захисту шкіри рук від подразнення під час ручного прання милом їх миють водою, до якої додають: а) кухонну сіль; б) етиловий спирт; в) питну соду; г) харчовий оцет.
5. При пранні виробів, що мають забруднення біологічного походження, наприклад плями крові, використовують засоби, що містять ферменти. Чи можна користуватись ними при пранні у дуже гарячій воді?
Подискутуйте
1. Враховуючу хімічні властивості білків, визначте порядок миття посуду з-під молока: а) миють гарячою, а потім холодною водою; б) витирають насухо і миють гарячою водою; в) миють холодною, а потім гарячою водою.
2. Чому мило «щипає» очі?
