Хімія. Повторне видання. 9 клас. Григорович
Цей підручник можна завантажити у PDF форматі на сайті тут.
§ 12. Реакції обміну між розчинами електролітів. Йонно-молекулярні рівняння хімічних реакцій
Йонно-молекулярні рівняння реакцій
Як ви вже вивчали у 8 класі, реакції обміну між солями, кислотами й основами в розчинах відбуваються за умови, що в результаті реакції:
- утворюється вода;
- випадає осад (нерозчинна у воді речовина);
- виділяється газ.
Розгляньмо, як відбуваються реакції обміну між розчинами електролітів, з позицій теорії електролітичної дисоціації. Для цього складають йонно-молекулярні рівняння: в молекулярному рівнянні реакції формули сильних електролітів замінюють формулами йонів, на які дисоціюють ці електроліти, а інші речовини (осади, гази, слабкі електроліти, оксиди тощо) — залишають у молекулярній формі.
Складемо йонно-молекулярне рівняння реакції нейтралізації хлоридної кислоти натрій гідроксидом. Спочатку записуємо молекулярне рівняння цієї реакції:
НСl + NaOH = NaCl + Н2О
Реагенти й один із продуктів реакції — це сильні електроліти. У водному розчині вони містяться винятково у вигляді йонів, а вода на йони майже не дисоціює. Зважаючи на це, замінюємо формули сильних електролітів формулами йонів:
H+ + Cl- + Na+ + ОН- = Na+ + Сl- + Н2О
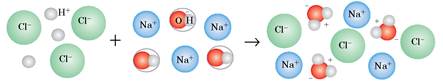
Такий запис називають повним йонно-молекулярним рівнянням реакції. У ньому записані всі частинки, що реально містяться в розчині. Із цього рівняння видно, що йони Сl- і Na+ у реакції не беруть участі — вони записані і в лівій, і в правій частинах рівняння, тому їх можна вилучити (скоротити):
H+ + OH- = H2O
Ми отримали скорочене йонно-молекулярне рівняння реакції. Воно показує хімічну суть цієї реакції: якщо в розчині одночасно наявні йони Н+ і ОН-, вони взаємодіють один з одним, утворюючи слабкий електроліт — воду.
У такий спосіб можна скласти йонно-молекулярне рівняння для будь-якої реакції в розчині. Такі рівняння відображають реальний процес, що відбувається в розчині, оскільки частина йонів не бере участі в реакції.
Реакції обміну з утворенням води
Складемо йонно-молекулярне рівняння реакції сульфатної кислоти з калій гідроксидом. Зверніть увагу, що необхідно враховувати стехіометричні коефіцієнти:
H2SO4 + 2КОН = K2SO4 + 2Н2О
2Н+ + SO42- + 2К+ + 2ОН- = 2К+ + SO42- + 2Н2О — повне рівняння
2Н+ + 2ОН- = 2Н2О або Н+ + ОН- = Н2О — скорочене рівняння
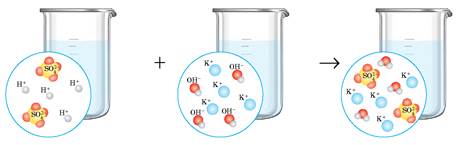
Як видно, повне йонно-молекулярне рівняння цієї реакції відрізняється від рівняння, складеного в попередньому підрозділі. Але скорочене йонно-молекулярне рівняння таке саме, як і для реакції хлоридної кислоти з натрій гідроксидом.
Обидві ці реакції є реакціями нейтралізації. Отже, хімічна суть реакцій нейтралізації полягає у сполученні йонів Н+ і ОН- у молекулу слабкого електроліту — води.
Розглянемо ще приклади взаємодії основ із кислотами.
Реакція між сульфатною кислотою й нерозчинним купрум(ІІ) гідроксидом:
H2SO4 + Cu(OH)2 = CuSO4 + 2Н2О
2Η+ + SO42- + Cu(OH)2 = Cu2+ + SO42- + 2H2O
2H+ + Cu(OH)2 = Cu2+ + 2H2O
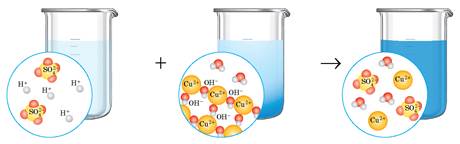
Взаємодія між слабкою сульфідною кислотою й калій гідроксидом:
H2S + 2КОН = K2S + 2Н2О
H2S + 2K+ + 2OH- = 2K+ + S2- + 2H2O
H2S + 2OH- = S2- + 2H2O
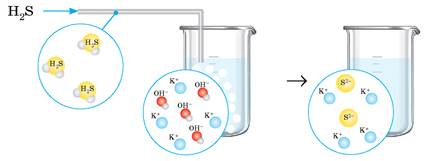
Зверніть увагу, у цих рівняннях формули слабких електролітів (Сu(ОН)2 та H2S) ми залишили в молекулярній формі, оскільки вони майже не дисоціюють на йони в розчині.
Реакції обміну з утворенням осаду
Розгляньмо реакцію обміну між розчинними солями:
ВаСl2 + Na2SO4 = BaSO4↓ + 2NaCl
Обидва реагенти й натрій хлорид — сильні електроліти, під час розчинення у воді вони повністю дисоціюють, а барій сульфат — нерозчинний:
Ва2+ + 2Сl- + 2Na++ SO42- = BaSO4↓ + 2Na+ + 2Сl-
Скорочене йонно-молекулярне рівняння отримуємо після вилучення однакових йонів у лівій і правій частинах:
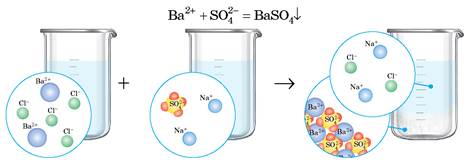
Отже, суть процесу полягає у взаємодії йонів Барію та сульфат-іонів з утворенням осаду барій сульфату.
Якщо в разі змішування розчинів двох розчинних солей осад не утворюється, то реакція не відбувається. Наприклад, під час зливання розчинів калій хлориду й магній сульфату жодних видимих змін не спостерігається. Запишемо рівняння цієї реакції обміну:
2КСl + MgSO4 = MgCl2 + K2SO4
Усі речовини — сильні електроліти:
2К+ + 2Сl- + Mg2+ + SO42- = Mg2+ + 2Сl- + 2К+ + SO42-
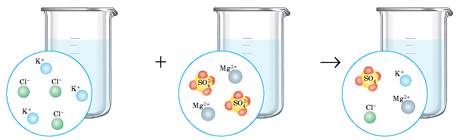
Бачимо, що ліва й права частини рівняння однакові, тобто утворений розчин містить усі йони, що були в розчинах реагентів.
Очевидно, що в цьому випадку ніякі йони один з одним не сполучаються, змін у розчині не відбувається. Це означає, що реакція неможлива:
КСl + MgSO4 ≠
Реакції обміну з виділенням газу
Газуваті речовини, що виділяються в реакціях обміну, зазвичай неелектроліти або слабкі електроліти. Тому під час складання йонно-молекулярних рівнянь їхні формули залишають у молекулярній формі.
Розглянемо реакцію натрій сульфіду з хлоридною кислотою:
Na2S + 2НСl = 2NaCl + H2S↑
Гідроген сульфід хоча і є кислотою, але дуже слабкою. До того ж гідроген сульфід погано розчиняється у воді, тому в разі утворення виділяється з розчину у вигляді газу, про що свідчить поява специфічного запаху сірководню — запаху тухлих яєць. Йонно-молекулярні рівняння цієї реакції:
2Na+ + S2- + 2Н+ + 2Сl- = 2Na+ + 2Сl- + H2S↑
S2- + 2H+ = H2S↑
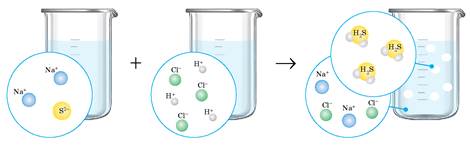
Реакції обміну можуть відбуватися навіть за участі нерозчинних у воді солей, якщо вони утворені слабкими кислотами: карбонатів, сульфітів і деяких сульфідів. Це можливо тому, що сильна кислота витісняє слабку з її солі, навіть із осаду.
Складемо рівняння взаємодії кальцій карбонату з хлоридною кислотою:
СаСО3 + 2НСl = СаСl2 + СО2↑ + Н2О
СаСО3 + 2Н+ + 2Сl- = Са2+ + 2Сl- + СО2↑ + Н2О
СаСО3 + 2Н+ = Са2+ + СО2↑ + Н2О
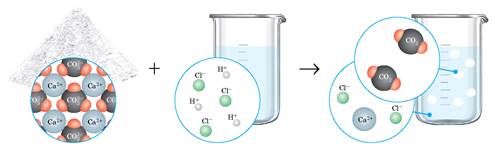
В усіх розглянутих випадках у результаті реакції обміну деякі йони сполучаються між собою, при цьому утворюються неелектроліти (гази) та слабкі електроліти (вода або нерозчинні речовини).
Реакції йонного обміну в розчинах відбуваються, якщо в результаті реакції утворюється слабкий електроліт або неелектроліт.
Відтворення молекулярних рівнянь за скороченим йонно-молекулярним рівнянням
Часто трапляються випадки, коли нам відоме тільки скорочене йонно-молекулярне рівняння, а необхідно визначити реагенти й скласти рівняння реакції в молекулярній формі.
Наприклад, нам необхідно здійснити хімічну реакцію, якій відповідає таке скорочене йонно-молекулярне рівняння:
S2- + 2Н+ = H2S↑
Для відтворення молекулярного рівняння необхідно визначити речовини, під час дисоціації яких утворюються йони з наведеного скороченого рівняння. Сульфід-іони S2- утворюються під час дисоціації розчинних сульфідів: Na2S, K2S та BaS.
Другий реагент має дисоціювати з утворенням йонів Н+. Цій умові відповідає будь-яка сильна кислота. Отже, одним із варіантів молекулярного рівняння є:
K2S + 2НВr = 2КВr + H2S↑
Звісно, що це не єдиний можливий варіант. Тому одному скороченому йонно-молекулярному рівнянню може відповідати декілька молекулярних. Таке вміння визначати реагенти стане вам у пригоді під час проведення лабораторних експериментів.
Реакції йонного обміну в розчинах відбуваються до кінця в бік зв'язування йонів, коли один із продуктів реакції виводиться з реакційного середовища. Розгляньмо реакцію між розчинами натрій хлориду й сульфатної кислоти:
2NaCl + H2SO4 ≠ Na2SO4 + 2НСl
Оскільки всі реагенти й продукти реакції добре розчинні та є сильними електролітами, то в розбавлених розчинах ця реакція не відбуватиметься. Але якщо реакцію проводити в умовах нестачі розчинника, тобто натрій хлорид узяти не у вигляді розчину, а в сухому, і сульфатну кислоту взяти у вигляді концентрованого розчину, то реакція можлива. Гідроген хлорид, хоча й добре розчиняється у воді, але обмежено:
NаСl(крист.) + Н2SО4(конц.) = NaHSO4 + НСl↑
