Хімія. Повторне видання. 8 клас. Григорович (2025)
§ 2. Формули та назви бінарних сполук

Чому хімічні формули саме такі, як їх пишуть
Поміркуйте
Що, на вашу думку, означає термін «бінарні сполуки»?
У 7-му класі ви вже дізналися, що склад речовин описують хімічними формулами, на кшталт згаданих Н2О або СО2. Вони саме такі, бо в цих речовинах так сполучені атоми Гідрогену й Карбону з атомами Оксигену.
У більшості речовин атоми хімічних елементів сполучені в певних відношеннях. Щоб дізнатися, які речовини можуть утворитися, треба розуміти, як атоми можуть взаємодіяти один з одним.
Ви вже знаєте, що атоми можуть перетворюватися на йони: катіони (позитивно заряджені) й аніони (негативно заряджені).
![]()
Протилежно заряджені йони притягуються один до одного
Однойменно заряджені йони відштовхуються один від одного
Приміром, атоми Натрію утворюють катіони із зарядом 1+, а атоми Хлору — аніони із зарядом 1-. Ці йони притягуються один до одного, утворюючи сполуку з формулою NaCl — кухонну сіль.

Якщо заряд 1+ або 1-, у позначенні йонів «1» зазвичай не записують
Аніони Хлору також утворюють сполуку з катіонами Кальцію, які мають заряд 2+. Будь-яка речовина є електронейтральною, а для цього кількість позитивних і негативних зарядів у речовині має бути однаковою.

Для нейтралізації заряду одного катіона Кальцію необхідно два аніони Хлору
![]()
Отже, у формулі сполуки ми записуємо символи одного атома Кальцію та двох атомів Хлору
За принципом електронейтральності можна складати формули бінарних сполук — сполук, що складаються з атомів двох хімічних елементів.
Пригадайте
Формули яких бінарних сполук ви пам'ятаєте з курсу хімії 7-го класу?
Важливо! Знаючи заряди, добираємо індекси у формулі сполуки так, щоб кількості позитивних і негативних зарядів були однакові.
Алгоритм: складаємо формули бінарних сполук за значеннями зарядів йонів
|
1. Записуємо символи хімічних елементів: першим пишемо з позитивним зарядом, а другим — із негативним, і надписуємо заряди |
Al3+S2- |
|
2. Визначаємо найменше спільне кратне (НСК) для значень зарядів (за модулем) |
НСК (3 і 2) = 6 |
|
3. Результат ділення НСК на заряд (за модулем) дорівнює індексу цього елемента у формулі |
6 : 3 = 2 (Аl) 6 : 2 = 3 (S) |
|
4. Записуємо індекси після символів хімічних елементів |
Al3+2S2-3 |
Як дізнатися заряди йонів?
Щоб визначати заряди йонів для всіх хімічних елементів, слід знати певні хімічні закономірності. Почнемо з найпростіших випадків.
Пригадайте
Як за розміщенням хімічного елемента в Періодичній таблиці дізнатися, є він металічним чи неметалічним?
Атоми металічних елементів можуть лише віддавати електрони, тож для йонів металічних елементів характерні тільки позитивні заряди.
І навпаки, атоми неметалічних елементів у хімічних реакціях переважно приєднують електрони та перетворюються на аніони1.
1 Неметалічні елементи можуть і віддавати електрони, але про це ви дізнаєтеся на наступних уроках.
Визначити заряди йонів, утворених з атомів деяких хімічних елементів можна за схемою.
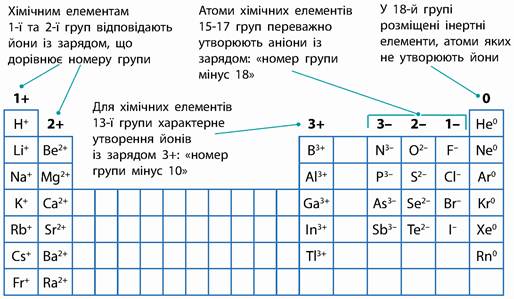
Чи є в речовин імена?
Минулого року ви ознайомилися з багатьма речовинами й знаєте їхні назви: вода, вуглекислий газ, кухонна сіль, метан тощо. Ці назви склалися історично і є традиційними. Але для всіх речовин, які існуюють у природі, навряд чи можна придумати, а тим паче запам’ятати мільйони традиційних назв. Тому в хімії існують правила складання назв речовин — хімічна номенклатура (від лат. nomenclatura — називальник імен). Ці правила рекомендує міжнародна спілка IUPAC (та сама, яка затверджує назви хімічних елементів). Назви речовин, складені за правилами хімічної номенклатури, називають систематичними.
Для складання систематичних назв бінарних сполук існує правило.


Назви одноатомних аніонів утворюються від назв відповідних хімічних елементів і суфікса -ид (-ід).
|
Хімічний елемент |
Назва елемента |
Назва аніона |
|
O |
Оксиген |
оксид |
|
N |
Нітроген |
нітрид |
|
Р |
Фосфор |
фосфід |
|
S |
Сульфур |
сульфід |
|
F |
Флуор |
флуорид |
|
Сl |
Хлор |
хлорид |
|
Вr |
Бром |
бромід |
|
I |
Йод |
Йодид |
У назвах речовин йонної будови зазначають заряд катіона (для тих хімічних елементів, заряди яких не можливо визначити за схемою на с. 21).
До прикладу:
FeCl2 — ферум(2+) хлорид; Ag2S — аргентум(1+) сульфід.
Катіони металічних хімічних елементів із великими зарядами (4+ і більше) зазвичай самі по собі не існують, тому для них указують формальний заряд1, який у назвах і формулах позначають римськими цифрами:
Ві2О5 — бісмут(V) оксид; SnCl4 — станум(ІV) хлорид.
1 Формальний заряд ще називають ступенем окиснення, про значення якого детальніше ви дізнаєтеся пізніше.
Зверніть увагу!
Важливо не плутати назву речовини та її вимову. Так, систематична назва води — гідроген оксид, а «аш-два-о» — це вимова її формули.

Досліджуємо, моделюємо, проєктуємо
За матеріалом параграфа створіть алгоритми:
- складання формули речовини за її назвою;
- визначення зарядів катіона й аніона в бінарній сполуці за формулою речовини.
Дізнайтеся більше
Суфікс -ід (-ид) у назвах бінарних сполук з'явився від латинського слова eidos — різновид. Наприклад, оксид (oxide) — це скорочено oxygen eidos — у перекладі буквально «сполука (різновид сполук) з Оксигеном».
Робота з інформацією
7. Із додаткових джерел дізнайтеся про речовини дальтоніди й бертоліди. Чим вони різняться та чому їх так називають?
8. Поясніть, що означає принцип електронейтральності, зокрема для складання формул бінарних сполук.
9. Запишіть назви аніонів, утворених хімічними елементами: С, Si, Se, Те, As.
10. Латинською binarius — той, що складається з двох, подвійний (від bini — «по два» та bis — «двічі»). Поясніть значення термінів «бінарна сполука», «бінарний код», а також виразу «зіграти щось на біс».
11. Складіть формули та систематичні назви сполук, утворених хімічними елементами: а) Н і S; б) К і S; в) Ва і F; г) Аl і I; д) Mg і Р; е) Na і N; є) Na і О; ж) К і Р.
12. Складіть систематичні назви сполук: К2О, Al2S3, Са3Р2, MgCl2, LiBr, NaI, HBr, FeF2, Cr2O3, PbCl4.
13. У більшості формул спочатку записують символ хімічного елемента з позитивним зарядом, але в деяких формулах, за традицією, пишуть навпаки. Зважаючи на це, складіть хімічні формули сполук із Гідрогеном: амоніаку, фосфіну, арсину та стибіну. Амоніак — це сполука Гідрогену з Нітрогеном. Визначте за назвами інших сполук, з атомами яких хімічних елементів у них сполучені атоми Гідрогену.

