Хімія. Профільний рівень. 11 клас. Григорович
§ 4. Особливості будови атомів у збудженому електронному стані. Валентність. Ступінь окиснення

Пригадайте:
- валентність — кількість хімічних зв'язків, які певний атом може утворити з іншими атомами;
- ступінь окиснення — це умовний заряд на атомі в молекулі або кристалі, який виник би на ньому, якби всі полярні зв'язки, утворені ним, мали йонний характер;
- електронегативність — здатність атомів притягувати спільну електронну пару; найбільша електронегативність в атомів Флуору, а найменша — в атомів Францію.
Збуджений стан атома
Зазвичай, коли ми говоримо про атоми чи молекули, йдеться про їхній основний енергетичний стан.
Основним називають такий стан атома (молекули), в якому енергія атома (молекули) мінімальна. У більшості випадків ця енергія визначається розподілом електронів в електронній оболонці згідно з принципом мінімальної енергії.
Будь-який енергетичний стан, що відрізняється від основного, називають збудженим. У такий стан атоми (молекули) можуть переходити за певних умов: під час нагрівання, за умови поглинання електромагнітного випромінювання (видимого, ультрафіолетового тощо).
Під час збудження атомів відбувається перехід електронів на інші, менш енергетично вигідні орбіталі. Наприклад, під час збудження атомів Гідрогену та Гелію електрони переходять на наступні енергетичні рівні (збуджений стан позначають зірочкою):
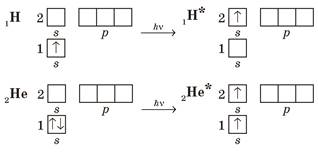
Для таких електронних переходів потрібно дуже багато енергії. Приміром, для збудження атомів Гідрогену їх необхідно опромінити жорстким ультрафіолетовим випромінюванням (так званий вакуумний ультрафіолет) або нагріти приблизно до температури 35 000 К (температура поверхні Сонця 6000 К).
Різниця енергій орбіталей одного енергетичного рівня набагато менша, тому атоми всіх інших неметалічних елементів переходять у збуджений стан набагато легше, для цього необхідна енергія, порівнянна з енергією хімічних реакцій. Так, під час збудження атома Карбону відбувається розпарування електронної пари і перехід електрона на вільну р-орбіталь того самого енергетичного рівня:
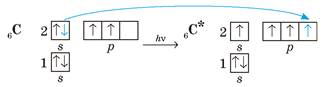
Атоми металічних елементів прагнуть віддавати електрони й легко переходять у збуджений стан. Настільки легко, що в багатьох випадках навіть відбувається втрата електрона зовнішнього рівня і перетворення атомів на йони.
В основному стані атоми можуть перебувати нескінченно довго, а в збудженому — лише частки секунди (близько 10-8-10-10 с). Збуджені атоми можуть утратити енергію і перейти в основний стан або сполучитися з іншими атомами й увійти до складу іншої частинки (молекули).
Валентні стани елементів
Валентністю називають кількість хімічних зв’язків, які атом утворює з іншими атомами в молекулі, тобто валентність дорівнює кількості спільних електронних пар, утворених атомом. Але спільні електронні пари характерні лише для ковалентного зв’язку.
У більшості випадків валентність визначається кількістю неспарених електронів в атомі. Наприклад, атоми Оксигену на зовнішньому енергетичному рівні містять два неспарені електрони, тому виявляють валентність II.
Кількість неспарених електронів в атомах може змінюватися внаслідок збудження атомів, завдяки чому атоми багатьох елементів виявляють змінну валентність.
В атома Хлору в основному стані на зовнішньому рівні один неспарений електрон, за допомогою якого він утворює один хімічний зв’язок, отже, виявляє валентність І. Поглинаючи енергію, один з електронів пари переходить на вільну d-орбіталь:
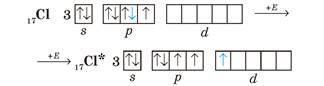
Унаслідок цього в атомі Хлору є вже три неспарені електрони, отже, він виявляє валентність III. Але і в цьому випадку на зовнішньому енергетичному рівні атома Хлору залишаються дві електронні пари і вільні d-орбіталі. Тому за умови поглинання додаткової енергії можливий перехід інших електронів на вільні орбіталі, завдяки чому Хлор може виявляти валентність V, а також і свою вищу валентність — VII:
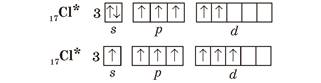
Так можна визначити всі можливі валентності для більшості елементів (табл. 1). Слід зауважити, що на зовнішньому енергетичному рівні атомів Нітрогену, Оксигену та Флуору вільні орбіталі відсутні, тому збільшення кількості неспарених електронів для них неможливе.
Можливі ступені окиснення елементів
Для всіх елементів у неорганічних речовинах незалежно від типу хімічних зв’язків застосовують універсальне поняття — ступінь окиснення. Це формальний заряд, який виник би, якщо вважати (припускати), що атом прийняв або віддав певну кількість електронів.
Атоми металічних елементів можуть тільки віддавати електрони, тому в сполуках вони виявляють позитивний ступінь окиснення. Його значення в багатьох випадках (за винятком d-елементів) дорівнює кількості електронів на зовнішньому рівні, а отже, і номеру групи в Періодичній системі (короткому варіанті).
Таблиця 1. Можливі валентності s- та p-елементів, визначені за будовою атома
|
Група ПС* |
І |
II |
III |
IV |
V |
VI |
VII |
|
Вища валентність |
І |
II |
III |
IV |
V (крім N) |
VI (крім О) |
VII (крім F) |
|
Можливі валентності |
- |
- |
- |
II (крім С) |
III |
II, IV |
I, IIІ, V |
* за коротким варіантом
Атоми неметалічних елементів можуть виявляти як позитивний, так і негативний ступінь окиснення залежно від того, з атомом якого елемента вони утворюють зв’язок. Якщо елемент більш електронегативний, то його атоми приймають електрони і він виявляє негативний ступінь окиснення, і навпаки.
Ви вже вивчали у 8 класі, що найбільш стабільними є електронні конфігурації інертних елементів, на зовнішньому енергетичному рівні яких міститься вісім електронів (октет Льюіса). Атоми всіх інших елементів прагнуть віддати або прийняти електрони, щоб утворити октет на зовнішньому енергетичному рівні.
• Ступені окиснення неметалічних елементів у разі прийому електронів
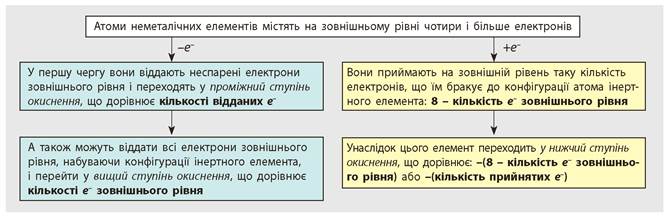
Атоми неметалічних елементів на зовнішньому енергетичному рівні містять чотири і більше електронів, тому вони насамперед прагнуть прийняти електрони на зовнішній рівень, щоб набути електронної конфігурації атомів інертного елемента. Наприклад, в атома Флуору на зовнішньому рівні сім електронів, він може прийняти до октету лише один електрон, унаслідок чого він переходить у ступінь окиснення -1, що є нижчим для Флуору:

У цьому процесі частинка стає більш стабільною, отже, її енергія знижується.
Якщо до октету бракує більше електронів, то нижчий ступінь окиснення буде іншим:
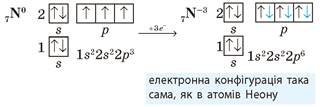
• Ступені окиснення неметалічних елементів у разі втрати електронів
Утворюючи зв’язок із більш електронегативним елементом, атоми неметалічних елементів частково втрачають електрони зовнішнього рівня, через що на них виникає позитивний заряд. Проте електрони все одно перебувають у спільних електронних парах і належать обом атомам, між якими виникає зв'язок, який вкотре демонструє, що ступінь окиснення - це умовний заряд. Насамперед в утворенні зв'язків беруть участь неспарені електрони, які є більш рухомими. Наприклад, в атомів Карбону на зовнішньому рівні два неспарені електрони, саме їх він може віддати в першу чергу, внаслідок чого переходить у ступінь окиснення +2:
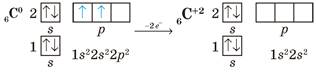
Якщо атом Карбону перебуває в збудженому стані, то він віддає всі електрони із зовнішнього рівня і переходить у ступінь окиснення +4, що є вищим для Карбону, набуваючи електронної конфігурації атомів інертного елемента:
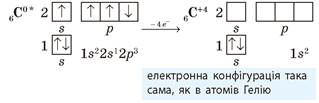
Оскільки кількість електронів на зовнішньому рівні збігається з номером групи (для короткого варіанта ПС), то вищий ступінь окиснення неметалічних елементів дорівнює номеру групи (крім Флуору й Оксигену).
У розглянутий спосіб можна визначити майже всі можливі ступені окиснення для s- та p-елементів (табл. 2).
Отже, для визначення можливих ступенів окиснення неметалічних елементів можна скористатися загальною схемою, наведеною на с. 14.
Таблиця 2. Можливі ступені окиснення s- і р-елементів
|
Група ПС |
І |
II |
III |
IV |
V |
VI |
VII |
VIII |
|
Вищий ступінь окиснення |
+1 |
+2 |
+3 |
+4 |
+5 |
+6 (крім О) |
+7 (крім F) |
0 |
|
Проміжний ступінь окиснення |
+2, 0 |
+3, 0 |
+4, +2, 0 |
+5, +3, +1, 0 |
0 |
|||
|
Нижчий ступінь окиснення |
0 |
0 |
0 |
-4 |
-3 |
-2 |
-1 |
0 |
Ключова ідея
Будова зовнішнього енергетичного рівня атомів зумовлює можливі валентні стани та ступені окиснення хімічних елементів, а отже, й можливі хімічні сполуки, що вони утворюють.
Запитання та завдання
15. Що називають основним і збудженим станами атомів? Що відбувається з електронами в електронній оболонці атомів під час збудження атома? Які енергетичні рівні та орбіталі можуть бути в цьому задіяні?
16. Дайте визначення понять «валентність» та «ступінь окиснення»? Що між ними спільного і чим вони відрізняються?
17. Поясніть, як можна за місцем хімічних елементів у Періодичній системі визначити їх можливі валентності та ступені окиснення.
18. Складіть електронні графічні формули атома Феруму в збудженому стані, у якому він може виявляти ступені окиснення +2 та +3.
19. За будовою електронної оболонки атомів визначте найхарактерніші валентності й ступені окиснення: а) Рубідію; б) Стронцію; в) Фосфору; г) Брому; д) Арсену.
20. Визначте ступені окиснення елементів у речовинах; СН4, NH3, H2S, НСІ, СаН2, AIF3, ВаСl2, CaS, К3Р, I2, N2O3, РbСl4, Сl2О7, ВrI3, NaF, Р4, CuI2, MgS, CF4, Са, CS2, Аl4С3, РСl5, Fe2S3.
