Хімія. 8 клас. Дячук
Цей підручник можна завантажити у PDF форматі на сайті тут.
Розділ 4. Основні класи неорганічних сполук
- Оксиди
- Основи
- Кислоти
- Солі
- Властивості оксидів
- Розрахунки за хімічними рівняннями
- Властивості основ
- Властивості кислот
- Властивості солей
- Амфотерні гідроксиди
- Добування оксидів
- Добування основ і амфотерних гідроксидів
- Добування кислот
- Добування солей
- Генетичні зв'язки між основними класами неорганічних сполук

Як ви пам'ятаєте з курсу хімії 7 класу, всі речовини поділяють на органічні і неорганічні. До органічних речовин належать майже всі сполуки Карбону. Неорганічні речовини — це прості речовини, а також речовини, утворені іншими елементами.
На даний час відомо близько 800 000 неорганічних речовин. Щоб орієнтуватися у такій величезній кількості речовин, їх поділяють на окремі класи — оксиди, основи, амфотерні гідроксиди, кислоти і солі.

Склад, властивості, поширеність у природі, використання та вплив на довкілля неорганічних речовин ми й будемо вивчати у наступних параграфах.
§ 25. Оксиди
Опрацювавши параграф, ви:
- повторите, які речовини називають оксидами;
- дізнаєтеся, як утворюють назви оксидів;
- навчитеся складати формули оксидів за їхніми назвами;
- дізнаєтеся, де використовують оксиди.
1. Склад і назви оксидів
Пригадайте з курсу хімії 7 класу, що
оксиди — сполуки, утворені двома хімічними елементами, одним із яких є оксиген.
У формулах оксидів символ Оксигену записують на другому місці.
В оксидах атоми Оксигену сполучаються з атомами інших елементів і не сполучаються між собою:

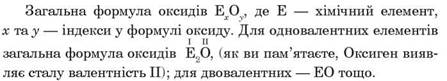
• Складіть загальну формулу оксидів елементів, які виявляють валентність V і VII.
Ступінь окиснення Оксигену в оксидах дорівнює -2:
![]()
Майже всі хімічні елементи утворюють оксиди. Винятками є Флуор і три інертні елементи — Гелій, Неон, Аргон.
Назви оксидів елементів, які мають постійну валентність, складаються з двох слів: назви елемента і слова «оксид», наприклад: MgO — магній оксид, Na2O — натрій оксид.
• Дайте назви таким оксидам: K2O, CaO, Al2O3.
Складіть формули оксидів за їхніми назвами: барій оксид, літій оксид, бор оксид.
Якщо елемент утворює декілька оксидів, то у назві римською цифрою в дужках вказують значення валентності елемента, наприклад:
MnO — манган(ІІ) оксид
Mn2O3 — манган(ІІІ) оксид
MnO2 — манган(IV) оксид.
• Дайте назви таким оксидам: Cu2O, CuO, FeO, Fe2O3.
Якщо валентність хімічного елемента в оксиді збігається з номером групи, у якій він розміщений, то оксид називають вищим: CO2 — карбон(ІV) оксид (вищий оксид Карбону), SO3 — сульфур(VІ) оксид (вищий оксид Сульфуру), P2O5 — фосфор(V) оксид (вищий оксид Фосфору).
• Складіть формули вищих оксидів Арсену і Селену.
2. Поширеність оксидів у природі
Найпоширенішим оксидом на Землі є гідроген оксид — вода. Вона наповнює океани, моря, озера й річки, пара води входить до складу повітря. Вода міститься в організмах тварин і рослин (мал. 32).

Мал. 32. Вода
Силіцій(ІV) оксид є у природі у вигляді піску (мал. 33). Як правило, пісок забруднений домішками (оксидами Феруму), які надають йому жовтого забарвлення.

Мал. 33. Пісок
Чисті кристали силіцій(ІV) оксиду називають кварцом, вони прозорі і безбарвні. У природі зустрічаються великі кристали кварцу (гірського кришталю) (мал. 34).

Мал. 34. Гірський кришталь
Кристалики SiO2 у вигляді включень є в граніті та інших гірських породах, при руйнуванні яких утворюється пісок.
До складу глини входять силіцій(IV) оксид SiO2 та алюміній оксид Al2O3. Дуже поширені у природі залізні руди — оксиди Феруму: Fe2O3, Fe3O4 (мал. 35).

Мал. 35. Залізні руди
У повітрі міститься невелика кількість вуглекислого газу (карбон(IV) оксиду. Сірчистий газ (сульфур(IV) оксид) є у вулканічних газах (мал. 36).

Мал. 36. Вулкан
3. Використання оксидів
Вода відіграє унікальну роль як речовина, яка визначає можливість існування і саме життя природи на Землі. Вона впливає на клімат, є середовищем, в якому відбуваються усі процеси в живих організмах. Велике значення має вода у промисловості, для транспорту, у будівництві. Особливо багато води потребують хімічна промисловість, металургійні підприємства, текстильні фабрики, цукрові заводи. Багато води витрачається у побуті.
З оксидів Феруму Fe2O3, Fe3O4 (вони є у складі залізних руд) добувають залізо. Кальцій оксид СаО використовують для одержання гашеного вапна. Цинк оксид ZnO використовують для виготовлення білої фарби, хром(ІІІ) оксид Cr2O3 — зеленої, ферум(ІІІ) оксид Fe2O3 — коричневої. Силіцій(IV) оксид SiO2 застосовують у будівництві. Прозорі кристали корунду Al2O3 використовують у ювелірній промисловості як дорогоцінні камені: рубін — червоного кольору (мал. 37), сапфір — синього кольору (мал. 38). Непрозорі кристали корунду застосовують для виготовлення шліфувальних матеріалів. Карбон(ІІ) оксид СО використовують як відновник під час виплавки металів і як паливо. Карбон(IV) оксид СО2 використовують під час виробництва газованих напоїв.

Мал. 37. Рубін

Мал. 38. Сапфір
• Якщо хочете знати хімію глибше...

• ...інколи у назві оксиду зазначають кількість атомів Оксигену за допомогою грецького числівника, наприклад:
СО — карбон монооксид;
СО2 — карбон діоксид;
SO2 — сульфур діоксид;
SO3 — сульфур триоксид.
• ...деякі оксиди мають ще й тривіальні назви, наприклад: CO — чадний газ, CO2 — вуглекислий газ, SO2 — сірчистий газ), CaO — палене або негашене вапно, MgO — палена магнезія.
• ...деякі хімічні елементи утворюють оксиди різних типів. Наприклад, CrO (нижча валентність ІІ) — основний оксид; Cr2O3 (валентність ІІІ) — амфотерний оксид; CrO3 (вища валентність VI) — кислотний оксид. MnO (нижча валентність ІІ) — основний оксид, Mn2O7 (вища валентність VII) — кислотний оксид.
• ...кристали гірського кришталю іноді досягають великих розмірів, було знайдено кристал масою 70 т.
ВИСНОВКИ
• Оксиди — сполуки, утворені двома хімічними елементами, одним із яких є Оксиген.
• Назви оксидів складаються з назви елемента і слова «оксид». Якщо елемент має змінну валентність, то у назві після назви елемента у дужках зазначають його валентність.
• Оксиди поширені у природі і використовуються у різних сферах діяльності людини.
Початковий рівень
1. Як поділяють речовини?
2. Як класифікують неорганічні речовини?
3. Укажіть хімічний елемент, що обов'язково входить до складу оксидів:
- А) Нітроген
- Б) Карбон
- В) Оксиген
- Г) Гідроген
4. У поданому переліку укажіть формули оксидів: KNO3, NO2, CaO, CaSO4, SO3, K2O, CaCl2, Cl2O, MgCO3, MgO.
5. Укажіть формулу хром(ІІІ) оксиду:
- А) CrO
- Б) Cr2O3
- В) Cr(OH)3
- Г) CrO3
6. Укажіть формулу нітроген(ІІ) оксиду:
- А) N2O
- Б) N2O5
- В) N2O3
- Г) NO
Середній рівень
7. Напишіть формули оксидів Літію, Селену(IV), Барію, Хрому(II), Натрію, Хрому(III), Карбону(II), Феруму(III), Мангану(IV), Фосфору(V), Карбону(ІV), Феруму(II).
8. Запишіть формули сполук, що мають такі назви: а) нітроген(II) оксид; б) фосфор(III) оксид; в) бор оксид; г) арсен(V) оксид.
9. Дайте хімічні назви таким оксидам: SnO, SnO2, PbO, PbO2, FeO, Fe2O3, WO, WO3.
10. Укажіть формулу вищого оксиду Сульфуру:
- А) SO3
- Б) SO2
- В) SiO2
- Г) H2SO3
11. Укажіть формулу вищого оксиду Хлору:
- А) Cl2O7
- Б) Cl2O
- В) Cl2O5
- Г) ClO2
12. Укажіть загальну формулу оксидів елементів головної підгрупи II групи:
- А) E2O
- Б) E2O3
- В) EO
- Г) EO3
13. Укажіть загальну формулу, якій відповідає оксид елемента із зарядом ядра атома +13:
- А) EO4
- Б) EO
- В) E2O5
- Г) E2O3
14. Укажіть загальну формулу, якій відповідає оксид елемента, розміщеного у головній підгрупі IV групи 3 періоду:
- А) EO2
- Б) E2O
- В) EO3
- Г) E2O3
15. Обчисліть ступені окиснення Сульфуру в SO2 і SO3.
16. Розмістіть оксиди у порядку зростання ступеня окиснення хімічних елементів, сполучених з Оксигеном:
- А) Li2O
- Б) CO2
- В) B2O3
- Г) CaO
17. Обчисліть масу купрум(ІІ) оксиду кількістю речовини 0,5 моль.
Достатній рівень
18. Укажіть електронну формулу атома елемента, який утворює оксид складу Е2О:
- А) 1s22s1
- Б) 1s22s22p63s2
- В) 1s22s22p63s23p64s2
- Г) 1s22s22p63s23p5
19. Укажіть електронну формулу атома елемента, який утворює оксид складу ЕО:
- А) 1s22s22p63s23p5
- Б) 1s22s22p63s23p64s2
- В) 1s22s22p63s23p64sx
- Г) 1s22s22p3
20. Обчисліть масу карбон(ІІ) оксиду об'ємом 5,6 л (н.у.)
21. Обчисліть об'єм (н.у.), який займають 2,408 · 1023молекул сульфур(ІV) оксиду.
22. Обчисліть відносну густину карбон(ІV) оксиду за воднем.
23. Укажіть відповідність між кількістю речовини оксиду і його масою:
Кількість речовини оксиду
- 1) 0,5 моль літій оксиду
- 2) 0,1 моль барій оксиду
- 3) 0,2 моль ферум(ІІ) оксиду
- 4) 0,1 моль ферум(ІІІ) оксиду
Маса оксиду
- A) 15 г
- Б) 14,4 г
- B) 16 г
- Г) 15,3 г
- Д) 16,5 г
24. Укажіть відповідність між об'ємом газуватого оксиду і його масою:
Об'єм оксиду
- 1) 5,6 л нітроген(І) оксиду
- 2) 11,2 л карбон(ІІ) оксиду
- 3) 5,6 л нітроген(ІІ) оксиду
- 4) 5,6 л сульфур(ІV) оксиду
Маса оксиду
- A) 14 г
- Б) 7,5 г
- B) 11 г
- Г) 11,5 г
- Д) 16 г
Високий рівень
25. Укажіть відповідність між кількістю речовини оксиду і кількістю речовини (моль) Оксигену, яку він містить:
Кількість речовини оксиду
- 1) 0,3 моль натрій оксиду
- 2) 0,2 моль кальцій оксиду
- 3) 0,2 моль алюміній оксиду
- 4) 0,1 моль фосфор(V) оксиду
Кількість речовини Оксигену (моль)
- A) 0,5
- Б) 0,4
- B) 0,2
- Г) 0,6
- Д) 0,3
26. Укажіть відповідність між об'ємом газуватого оксиду і кількістю речовини (моль) Оксигену, яку він містить:
Об'єм оксиду
- 1) 11,2 л сульсфур(IV) оксиду
- 2) 22,4 л карбон(ІV) оксиду
- 3) 5,6 л нітроген(ІV) оксиду
- 4) 67,2 л нітроген(ІІ) оксиду
Кількість речовини Оксигену (моль)
- А) 1
- Б) 2
- В) 3
- Г) 2,5
- Д) 0,5
27. Обчисліть масові частки елементів у вищому оксиді Фосфору.
28.* Вищий оксид деякого хімічного елемента головної підгрупи IV групи масою 22 г займає об'єм 11,2 л (н. у.). Визначте масову частку Оксигену у цьому оксиді.
Цей контент створено завдяки Міністерству освіти і науки України
