Хімія. Повторне видання. 8 клас. Ярошенко (2025)
§ 9. Кількісні відношення речовин у хімічних реакціях
• На основі якого закону складають рівняння хімічних реакцій?
• Наведи приклад хімічного рівняння і для кожної речовини назви індекси і коефіцієнти.
Опрацюй. Зрозумій. Використай
Тобі відомо, що коефіцієнти у хімічних рівняннях потрібні для того, щоб записувати перебіг хімічних явищ з дотриманням закону збереження маси в хімічних реакціях.
Формулюємо навчальну проблему та розв'язуємо її
Як коефіцієнти у хімічному рівнянні пов’язані з кількістю речовини реагентів / реактантів і продуктів реакції?
Розглянемо розв’язання проблеми на прикладі хімічного рівняння
N2 + 3H2 = 2NH3.
Одна молекула азоту взаємодіє з трьома молекулами водню, утворюючи дві молекули амоніаку.
Уявімо, що в реакцію вступає не одна молекула азоту, а 6,02 • 1023. Тоді водню прореагує 3 • 6,02 • 1023 = 18,06 • 1023 молекул, й утвориться 2 • 6,02 • 1023 = 12,04 • 1023 молекул амоніаку.
Оскільки 1 моль кожної речовини містить 6,02 • 1023 молекул, то кількість речовини реагентів і продукту реакції становить: 1 моль азоту, 3 моль водню, 2 моль амоніаку. Саме такі коефіцієнти наявні у рівнянні реакції.
Напишемо відношення кількості речовини реагентів / реактантів азоту та водню і продукту реакції амоніаку:
N2 + 3Н2 = 2NH3
1 моль : 3 моль : 2 моль
Медіапошук
Водний розчин амоніаку під назвою нашатирний спирт або аміаку розчин застосовується у фармації як лікувальний засіб (мал. 7).
Скористайся додатковими джерелами інформації та підготуй коротке повідомлення про застосування водного розчину амоніаку та його фізіологічну дію.

Мал. 7. Аміаку розчин 10 %
Коефіцієнти у хімічному рівнянні вказують на кількість речовини реагентів / реактантів і продуктів реакції.
Як тобі відомо, коефіцієнт 1 не пишеться. В такому разі запис формули без коефіцієнта означає 1 моль речовини.
Завдання. Перетвори схеми на хімічні рівняння, запиши та прокоментуй кількісні відношення речовин у них.
Аl + О2 → Al2O3
Н2O + Р2О5 → Н3РО4
ЯКІ РОЗРАХУНКИ МОЖНА ЗДІЙСНЮВАТИ ЗА КІЛЬКІСНИМИ ВІДНОШЕННЯМИ РЕЧОВИН У ХІМІЧНОМУ РІВНЯННІ?
За кількісними відношеннями речовин у хімічному рівнянні можна обчислювати масу і кількість речовини, об’єм газу (про останнє дізнаєшся в наступній темі). Такі обчислення проводять технологи хімічних виробництв, дослідники, студенти та учні на заняттях з хімії.
Варто пам’ятати: якою б не була маса взятих для проведення хімічної реакції реагентів, взаємодіятимуть вони та утворюватимуть продукти реакції у кількостях, що відповідають кількісному відношенню речовин у хімічному рівнянні.
Розглянемо приклади.
Приклад 1. Обчислимо масу водню, що прореагував з азотом кількістю речовини 4 моль.
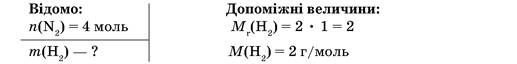
Розв’язання
1. Записуємо рівняння реакції:
N2 + 3Н2 = 2NH3.
2. Встановлюємо кількісні відношення азоту та водню за хімічним рівнянням та за умовою задачі.
|
Кількісні відношення речовин |
Кількість речовин |
|
|
азот Ν2 |
водень Н2 |
|
|
За рівнянням |
1 моль |
3 моль |
|
За умовою |
4 моль |
х моль |
|
n(Ν2) : n(Н2) = 1 : 3 |
||
Знайдене відношення свідчить: кількість речовини водню в 3 рази більша за кількість речовини азоту.
3. Обчислюємо кількість речовини водню.
Перший спосіб:
n(Н2) = 3 • n(N2) = 3 • 4=12 моль.
Другий спосіб:

4. За формулою m = n • М обчислюємо масу водню кількістю речовини 12 моль:
m(Н2) = 12 моль • 2 г/моль = 24 г.
Відповідь: маса водню дорівнює 24 г.
Приклад 2. Обчислимо масу кисню, що прореагував з магнієм з утворенням магній оксиду кількістю речовини 6 моль.

Розв’язання
1. Записуємо рівняння реакції:
2Mg + О2 = 2MgO.
2. Встановлюємо кількісні відношення кисню та магній оксиду за хімічним рівнянням та за умовою задачі.
|
Кількісні відношення речовин |
Кількість речовин |
|
|
кисень О2 |
магній оксид МgО |
|
|
За рівнянням |
1 моль |
2 моль |
|
За умовою |
x моль |
6 моль |
|
n(О2) : n(МgО) = 1 : 2 |
||
3. Обчислюємо кількість речовини кисню.
За кількісним відношенням кисню до магній оксиду кількість речовини кисню вдвічі менша, ніж магній оксиду. Тому за умовою задачі х буде вдвічі менше, ніж 6:
6 : 2 = 3 моль.
4. За формулою m = n • М обчислюємо масу кисню кількістю речовини 3 моль:
m(О2) = 3 моль • 32 г/моль = 96 г.
Відповідь: маса кисню дорівнює 96 г.
У хімічних реакціях взаємодія речовин відбувається не в довільній кількості, а відповідно до кількісних відношень речовин.
Перевага розрахунків з використанням кількісних відношень речовин у рівнянні полягає в тому, що увага концентрується на хімічному явищі, а не на математичних обчисленнях.
Нумо обчислювати
МАСУ ПРОДУКТУ РЕАКЦІЇ ЗА ХІМІЧНИМ РІВНЯННЯМ
Обчислення виконай у складі навчальної групи.
Завдання. Обчисліть, в якій хімічній реакції маса утвореного оксиду буде більшою:
- а) цинк кількістю речовини 4 моль прореагував без залишку з киснем;
- б) алюміній масою 56 г прореагував без залишку з киснем.
ХІМІЧНА СКАРБНИЦЯ
У цьому параграфі наведено приклади обчислення маси чи кількості речовини продукту реакції за хімічними рівняннями. Одержані результати називають теоретичним виходом речовини. В дійсності на виробництві чи в хімічній лабораторії з різних причин (недосконалість апаратури, недотримання умов проведення реакції, особливості перебігу хімічного процесу, недбалість працівників та інше) отримують продукту реакції менше, ніж обчислено теоретично. Реальний вихід називають практичним виходом.
Щоб розумітись на тому, наскільки хімічний процес продуктивний, введено поняття відносного виходу продукту реакції. Для хімічних виробництв його обчислення є необхідним і проводиться обов’язково.
Відносний вихід продукту реакції (η, читається «ета») обчислюють у частках від 1 або у відсотках від 100 за формулами:


ТОБІ ДО СНАГИ
1. Поясни, як встановити кількісні відношення речовин у хімічній реакції.
2. Запиши кількісні відношення речовин у хімічному рівнянні, схема якого ВаО + Аl → Ва + Аl2О3.
3. Реакція відбувається за схемою Cr2O3 + НСl → СrСl3 + Н2О. Розташуй формули речовин у порядку збільшення кількості речовини в рівнянні наведеної реакції.
4. Обчисли кількість речовини метану СН4, що утвориться у реакції вуглецю з воднем масою 80 г.
5. У якому випадку утворюється більша кількість продукту?
- А водень масою 16 г взаємодіє з киснем за схемою Н2 + О2 → Н2О;
- Б магній масою 24 г взаємодіє з киснем за схемою Mg + О2 → МgО.
6. Склади умову задачі на встановлення кількісних відношень речовин у хімічній реакції, щоб виконати його на уроці разом з учнівством.
