Хімія. Повторне видання. 8 клас. Ярошенко (2025)
§ 38. Моделі ковалентного хімічного зв'язку
• Наведи приклади неметалічних хімічних елементів.
• Пригадай формули двоатомних молекул простих речовин.
• Запиши графічні електронні формули атомів Карбону, Нітрогену, Оксигену, Флуору та Неону. Вияви тенденцію у заповненні електронами зовнішнього енергетичного рівня цих атомів.
Опрацюй. Зрозумій. Використай
Розглянуті в попередньому параграфі способи утворення завершеного зовнішнього енергетичного рівня електронної оболонки атома забезпечують існування того чи іншого виду хімічного зв’язку. Розпочнемо їх вивчення з ковалентного зв’язку. Для з’ясування його суті важливе значення має така фізична характеристика атома, як електронегативність.
ЕЛЕКТОРОНЕГАТИВНІСТЬ. Згідно з електронною теорією хімічного зв’язку в його утворенні головну роль відіграють електростатичні сили притягання, що діють між електронами та ядрами атомів. Для характеристики здатності атома притягувати до себе електрони інших атомів науковці ввели поняття електронегативності.
Електронегативність хімічного елемента — це властивість його атома притягувати електрони від інших атомів.
З урахуванням електронегативності укладено ряд електронегативності хімічних елементів, в якому кожний наступний хімічний елемент характеризується меншою електронегативністю за попередній:

Отже, Флуор — «абсолютний чемпіон» з електронегативності. Друге місце посідає Оксиген, третє — Хлор, четверте — Нітроген. Загалом неметалічні елементи мають значно більшу електронегативність, ніж металічні.
Завдання 1. За допомогою ряду електронегативності визнач, до якого елемента сильніше притягуються валентні електрони (так називають електрони, що беруть участь в утворенні хімічного зв’язку) в молекулах такого складу: НСl, CS2, NH3.
Завдання 2. Вислови свої припущення щодо зміщення валентних електронів у двоатомних молекулах кисню й азоту. Відшукай у тексті параграфа інформацію, що підтверджує або спростовує твої припущення.
ХІМІЧНА СКАРБНИЦЯ
Періодична залежність властивостей хімічних елементів проявляється і в електронегативності атомів. У періодах електронегативність атомів зі збільшенням заряду ядра атома зростає, а в головних підгрупах (коротка форма періодичної таблиці) — спадає. Це є ще одним підтвердженням універсальності періодичного закону.
ПОНЯТТЯ КОВАЛЕНТНОГО ЗВ’ЯЗКУ. В його утворенні беруть участь неспарені електрони. За рахунок перекривання їхніх атомних орбіталей два атоми утворюють спільну електронну пару (мал. 57).

Мал. 57. Модель утворення ковалентного зв’язку в молекулі водню
Місце перекривання електронних орбіталей має підвищену електронну густину, до якої притягуються позитивно заряджені ядра двох атомів. Приклад перекривання s-орбіталей ілюструє малюнок 58.

Мал. 58. Прекривання s-орбіталей з утворенням спільної електронної пари в молекулі водню
Хімічний зв’язок, що утворений за рахунок спільних електронних пар, називається ковалентним.
Ковалентний зв’язок існує між атомами неметалічних елементів. Важливо пам’ятати, що утворення спільних електронних пар відбувається лише з неспарених електронів. Кількість таких електронів, а отже, й утворюваних ними електронних пар, легко визначити за графічною електронною формулою атома. Перехід атома у збуджений стан збільшує кількість неспарених електронів, а отже, й хімічних зв’язків. Саме тому більшість хімічних елементів мають змінну валентність.
Утворена спільна електронна пара може бути рівно- чи різновіддалена від ядер зв’язаних з нею атомів. Від чого це залежить та який різновид ковалентного зв’язку утворюється у кожному випадку, розглянемо на конкретних прикладах.
МОДЕЛЬ КОВАЛЕНТНОГО НЕПОЛЯРНОГО ЗВ’ЯЗКУ НА ПРИКЛАДІ МОЛЕКУЛИ ХЛОРУ. Ковалентний зв’язок атомів з однаковою електронегативністю утворюється без зміщення електронних пар до одного з них, тому має назву ковалентний неполярний зв’язок.
Ковалентний неполярний зв’язок — це зв’язок, що утворений за рахунок спільних електронних пар, які рівновіддалені від ядер обох атомів.
Молекула хлору утворена двома атомами Хлору, електронна й графічна електронна формули яких —
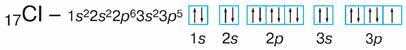
Як свідчить графічна електронна формула, атом Хлору має лише один неспарений електрон. Отже, незважаючи на наявність семи електронів на зовнішньому енергетичному рівні, атом Хлору може утворити лише одну спільну електронну пару:

На малюнку 59 показано перекривання р-орбіталей з утворенням спільної електронної пари в молекулі хлору.

Мал. 59. Схема перекривання р-орбіталей
Утворення хімічного зв’язку в молекулі хлору можна змоделювати за допомогою символу хімічного елемента Хлору та крапок, що позначають електрони зовнішнього енергетичного рівня його атома (мал. 60).

Мал. 60. Модель утворення ковалентного неполярного зв’язку в молекулі хлору
Модель ілюструє утворення атомами Хлору спільної електронної пари, яка рівновіддалена від ядер обох атомів. За рахунок цієї пари стає завершеним третій (зовнішній) енергетичний рівень кожного атома. Таку саму будову він має в інертного хімічного елемента Аргону. Це не збіг і не випадковість.
У молекулах з ковалентним зв’язком електронна оболонка кожного з атомів досягає будови інертного хімічного елемента, який розташований з ним в одному періоді.
МОДЕЛЬ КОВАЛЕНТНОГО ПОЛЯРНОГО ЗВ’ЯЗКУ НА ПРИКЛАДІ МОЛЕКУЛИ ГІДРОГЕН ХЛОРИДУ НСl. У молекулі гідроген хлориду хімічний зв’язок утворюється між атомами різних неметалічних елементів — Гідрогену й Хлору. Атоми кожного з них мають по одному неспареному електрону. За рахунок утворення ними спільної електронної пари зовнішній енергетичний рівень і Гідрогену, і Хлору стає завершеним (мал. 61).

Мал. 61. Модель утворення ковалентного полярного зв’язку в молекулі гідроген хлориду
Зверни увагу, що спільна електронна пара зміщена до атома Хлору.
Завдання 3. Чому в молекулі гідроген хлориду спільна електронна пара зміщується до Хлору? Скористайся рядом електронегативності для надання відповіді.
Хімічний зв’язок за допомогою спільних електронних пар, які зміщені до більш електронегативного атома, називається ковалентним полярним.
ПЛІЧ-О-ПЛІЧ
Завдання 1. Напишіть молекулярні та електронні формули кисню, азоту, метану, води. Складіть схеми утворення молекул кожної речовини з атомів.
Завдання 2. Змоделюйте утворення цих молекул.
Для цього вам знадобиться набір для створення моделей молекул , а за його відсутності — пластилінові кульки і дерев’яні палички (одна паличка моделюватиме спільну електронну пару).
Завдання 3. Розгляньте моделі й з’ясуйте:
3.1. У молекулі якої речовини найбільше ковалентних зв’язків.
3.2. Молекули яких речовин мають однакову кількість ковалентних зв’язків та в чому полягає їх відмінність.
Медіапошук
Ознайомся з механізмом утворення ковалентного зв’язку в молекулах гідроген хлориду (у відео використано тривіальну назву НСІ — хлороводень) і хлору за покликанням https://qr.orioncentr.com.ua/D5Iva.
Запропонуй власні ідеї моделювання утворення ковалентного зв’язку в молекулах фтору і гідроген фториду.

ТОБІ ДО СНАГИ
1. Яку властивість хімічних елементів називають електронегативністю?
2. Розташуй хімічні елементи за зростанням електронегативності
- А Алюміній
- Б Сульфур
- В Карбон
- Г Гідроген
3. Сформулюй визначення ковалентного зв’язку та поясни, чим полярний ковалентний зв’язок відрізняється від неполярного.
4. У якій із молекул: а) кисню; б) води; в) водню; г) гідроген броміду — спільні електронні пари зміщені до одного з атомів і чому?
5. Підготуй завдання з теми цього параграфа і запропонуй однокласникам / однокласницям виконати його.
6. Розмісти формули речовин за збільшенням кількості спільних електронних пар у молекулі.
- А Н2О
- Б СН4
- B HF
- Γ ΝΗ3
7. Доведи або спростуй твердження: «Ковалентний зв’язок може утворитись між однаковими або різними атомами».
8. Назви якомога більше відомих тобі спільних характеристик речовин: водню, фтору, хлору.
