Хімія. Повторне видання. 8 клас. Ярошенко (2025)
§ 35. Діагностування результатів вивчення теми 3 «Досліджуємо будову атома»
Матеріал параграфа дасть тобі змогу повторити та узагальнити вивчені в темі 3 будову атома й періодичний закон, діагностувати результати навчання під час виконання вправ та онлайн-тесту.
Виконай вправи
1. Поясни, що означає термін «субатомні частинки». Наведи приклади.
2. Як дізнатися про кількість субатомних частинок в атомі? Пояснення ілюструй на прикладі атома Алюмінію.
3. Порівняй за масою і зарядом: а) протон та електрон; б) протон і нейтрон.
4. Що розуміють під протонним числом, нуклонним / масовим числом?
5. Чи можуть ядра атомів, які мають однакове нуклонне / масове число, належати різним елементам? Поясни свою відповідь.
6. Увідповідни цифрові позначення на малюнку й підписи.
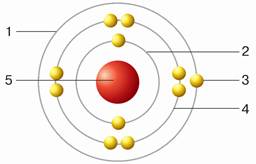
____ — неспарений електрон
____ — другий енергетичний рівень
____ — третій енергетичний рівень
____ — ядро атома
____ — перший енергетичний рівень
7. Атом має 12 протонів і 12 нейтронів. Обчисли масове число атома. Який це хімічний елемент?
8. Порівняй кількість субатомних частинок у нуклідах 2713Аl і 2913Аl.
9. Проаналізуй дані таблиці й укажи нукліди одного хімічного елемента.
|
Атом (умовне позначення) |
Кількість протонів |
Кількість електронів |
Кількість нейтронів |
|
А |
8 |
8 |
8 |
|
Б |
6 |
6 |
6 |
|
В |
8 |
8 |
9 |
Поясни свою відповідь.
10. Нуклід Брому має масове число 80 і містить 35 електронів. Скільки протонів і нейтронів у нукліда Брому та який заряд його ядра?
11. Поясни зміст понять «електронна орбіталь», «енергетичний рівень», «енергетичний підрівень».
12. Для атома елемента, який має 13 протонів, визнач кількість електронів і нейтронів, якщо масове число елемента 27. На яких енергетичних рівнях цього атома розташовані електрони?
13. Розташуй елементи в послідовності зменшення кількості електронів в атомі: Se, І, К, Fe, Cl, Li, S. Укажи елементи з однаковою кількістю енергетичних рівнів в електронній оболонці.
14. Заповни в зошиті таблицю.
|
Енергетичний рівень |
Максимальна кількість електронів на рівні |
Форми атомних орбіталей |
|
1 |
||
|
2 |
||
|
3 |
15. За схемою електронної оболонки атома

визнач хімічний елемент, напиши електронну формулу атома й укажи:
— заряд ядра;
— кількість енергетичних рівнів;
— номер періоду, в якому розміщений елемент;
— номер групи у довгій формі періодичної таблиці;
— номер групи і підгрупу в короткій формі періодичної таблиці;
— кількість електронів на зовнішньому енергетичному рівні;
— завершеним чи незавершеним є зовнішній енергетичний рівень.
16. Чому Натрій розміщений у третьому періоді, а Нітроген — у другому?
17. Користуючись схемою і науковою термінологією, порівняй будову атомів Магнію і Кальцію.

18. Що про будову атома можна дізнатись за його електронною оболонкою? Поясни на прикладі будь-якого елемента з 1-3 періодів.
19. Увідповідни схему електронної оболонки атома і період, в якому розміщений хімічний елемент.

20. Визнач хімічний елемент, зовнішня електронна оболонка якого має будову ...2s22p3. Для цього елемента:
- а) схарактеризуй місце в періодичній таблиці (короткій і довгій формах);
- б) сформулюй висновок щодо зв’язку будови атома й місця елемента в періодичній таблиці;
- в) назви відомі тобі речовини, до складу яких входить цей елемент, і галузі їх застосування.
Виконай онлайн-тест.
Для цього перейди за покликанням https://qr.orioncentr.com.ua/EWWr1 або скористайся смартфоном — зчитай QR-код.

Якщо результат виконання тесту тебе не задовольнить, можеш його покращити. Знайди можливість самостійно виправити помилки, яких припустився / припустилась, щоб уникнути їх у майбутньому.
Бажаємо успіху та високого результату!
