Хімія. Повторне видання. 8 клас. Ярошенко (2025)
§ 29. Розподіл електронів за енергетичними рівнями
• Назви енергетичні підрівні та максимально можливу кількість електронів на кожному з них.
• Які орбіталі є у складі 1-3-го енергетичних рівнів?
• Чи може бути на s-підрівні: а) 1 електрон; б) 2 електрони; в) 6 електронів?
• Чи може бути на р-підрівні: а) 1 електрон; б) 6 електронів; в) 8 електронів?
Опрацюй. Зрозумій. Використай
Існують певні правила розподілу електронів в атомі за енергетичними рівнями та підрівнями. Дотримуючись цих правил, записують електронні формули атомів (електронні конфігурації атомів).
ПОНЯТТЯ ПРО ЕЛЕКТРОННУ ФОРМУЛУ / КОНФІГУРАЦІЮ АТОМА. Характеризувати розподіл електронів в електронній оболонці атома за енергетичними рівнями та підрівнями зручно й нескладно за допомогою електронної формули атома (інша назва — електронна конфігурація атома).
Електронна формула / електронна конфігурація атома — це запис розподілу електронів в електронній оболонці атома за допомогою арабських чисел 1-7 (ними позначають енергетичні рівні), малих англійських літер s, р, d, f (енергетичні підрівні) та верхніх індексів після них (кількість електронів на підрівні).
Розглянемо це на прикладі електронної формули Карбону.
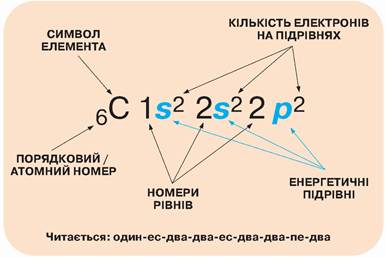
Порядковий номер 6 (протонне число, атомний номер) свідчить про наявність в електронній оболонці атома Карбону шести електронів. Якщо ми обчислимо суму верхніх індексів, що відповідають кількості електронів на підрівнях, то отримаємо 6. Арабські цифри 1 і 2 вказують на наявність двох енергетичних рівнів. Запис 1s2 означає, що на 1-му енергетичному рівні є 2 електрони, розміщені на підрівні s. Запис 2s22p2 інформує про існування на 2-му енергетичному рівні 4 електронів, розміщених на двох підрівнях, та кількість електронів на кожному з них.
Завдання. За зразком наведеної наукової інформації про розподіл електронів в електронній оболонці атома Карбону прочитай електронну формулу і прокоментуй розподіл електронів за рівнями і підрівнями в атомі Фосфору:
15Р 1s22s22p63s23p3.
ПРАВИЛА ЗАПОВНЕННЯ ЕЛЕКТРОНАМИ ЕНЕРГЕТИЧНИХ РІВНІВ ТА ПІДРІВНІВ. Час навчитись самим писати електронні формули атомів перших 20 хімічних елементів періодичної таблиці. Для цього варто дотримуватись зазначених нижче правил.
- 1. Кількість електронів в електронній оболонці атома дорівнює порядковому / атомному номеру хімічного елемента.
- 2. Кількість енергетичних рівнів / електронних шарів в електронній оболонці атома відповідає номеру періоду, в якому хімічний елемент розміщений у періодичній таблиці.
- 3. У кожного атома заповнення енергетичних рівнів електронами починається з 1-го енергетичного рівня. Він має лише один s-підрівень, на якому не може бути більше 2 електронів.
- 4. Після заповнення 1-го енергетичного рівня електрони заповнюють 2-й енергетичний рівень. Спочатку двома електронами заповнюється s-підрівень другого енергетичного рівня, після чого електронами заповнюється р-підрівень, на якому можуть перебувати від 1 до 6 електронів.
- 5. Максимальна кількість електронів на другому енергетичному рівні — вісім.
- 6. За розглянутими вище правилами розпочинається заповнення електронами третього енергетичного рівня електронної оболонки атомів хімічних елементів 3-го періоду. У хімічних елементів 3-го періоду його d-підрівень лишається незаповненим електронами.
Пригадай, що на d-підрівні можуть перебувати від 1 до 10 електронів. Його заповнення починається у Скандію Sc (порядковий номер 21) і закінчується у Цинку Zn (порядковий номер 30). Усе це елементи 4-го періоду, будову атомів яких ти вивчатимеш у профільній школі.
ПЛІЧ-О-ПЛІЧ
Завдання. Потренуйтеся складати електронні формули атомів і застосовувати їх для характеристики будови електронної оболонки атома.
- 1. Дотримуючись розглянутих загальних правил, напишіть і прочитайте електронні формули Гідрогену, Гелію, Літію, Нітрогену, Оксигену, Натрію, Сульфуру й Аргону.
- 2. Назвіть, які з них мають однакову кількість енергетичних рівнів.
- 3. Назвіть елементи з однаковою кількістю електронів на р-підрівнях.
- 4. Назвіть кількість електронів на внутрішньому енергетичному рівні кожного атома. Чи відрізняються розглянуті елементи за їх кількістю?
- 5. Сформулюйте висновок про те, якою є кількість електронів на 1-му енергетичному рівні.
- 6. Проаналізуйте електронні формули та зазначте, в атомах яких елементів 2-й енергетичний рівень максимально заповнений.
- 7. З’ясуйте, у якого з досліджуваних елементів р-підрівень усіх енергетичних рівнів максимально заповнений електронами.
НУМО ДОСЛІДЖУВАТИ
РОЗПОДІЛ ЕЛЕКТРОНІВ ЗА ЕНЕРГЕТИЧНИМИ РІВНЯМИ
Завдання 1. Перевір правильність відповідей учнів на завдання, наведені в таблиці 23. Порівняй їх зі своїми відповідями.
Таблиця 23
|
Номер |
Запитання й завдання |
Відповідь гіпотетичного учня/учениці |
Твоя відповідь |
|
1 |
Як, користуючись періодичною таблицею, визначити кількість енергетичних рівнів в електронній оболонці атома? |
Потрібно подивитись, у якій групі періодичної таблиці розташований елемент |
|
|
2 |
Як дізнатись про кількість електронів в електронній оболонці атома? |
Потрібно подивитись, який порядковий номер хімічного елемента у періодичній таблиці |
|
|
3 |
На якому енергетичному рівні перебувають електрони з більшим запасом енергії — на другому чи на третьому? |
Електрони з більшим запасом енергії перебувають на другому енергетичному рівні |
|
|
4 |
Скільки електронів на р-орбіталях в атома Фосфору? |
Дев’ять |
|
|
5 |
Напиши електронну формулу атома Магнію |
12Mg 1s22s32p53s13p1 |
Завдання 2. Доведи відповідями на запитання, що вмієш характеризувати розподіл електронів в атомах перших 20 хімічних елементів періодичної таблиці. Відповіді супроводжуй записом відповідних електронних формул.
- 2.1. У Літію чи Натрію всі електрони розташовані лише на s-підрівнях?
- 2.2. Атом Гідрогену чи Нітрогену має один енергетичний рівень?
- 2.3. Однакову чи різну кількість енергетичних рівнів мають Оксиген і Неон?
- 2.4. Електронна конфігурація якого хімічного елемента має закінчення ...3s23p4?
ТОБІ ДО СНАГИ
1. Сформулюй визначення понять: атомна орбіталь, енергетичний рівень, енергетичний підрівень, електронна формула.
2. Яку інформацію про будову електронної оболонки атома можна отримати з електронної формули атома?
3. В електронній оболонці атома три енергетичні рівні. На зовнішньому енергетичному рівні знаходиться 8 електронів. Назви хімічний елемент, напиши його електронну формулу.
4. В електронній конфігурації атома 6 електронів розміщені на s-орбіталях і 8 на р-орбіталях. За цією інформацією віднови і запиши електронну формулу атома. Назви хімічний елемент.
5. Електронна формула має закінчення ...4s1 у атома з порядковим номером...
- А 4
- Б 9
- В 11
- Г 19
6. Укажи якомога більше ознак, за якими укладено перелік хімічних елементів: Нітроген, Оксиген, Флуор.
7. За зразком завдань рубрики «Нумо досліджувати» склади 3-4 умови завдань і презентуй їх класу в самостійно обраний спосіб для виконання.
