Хімія. Повторне видання. 8 клас. Ярошенко (2025)
Тема 3. Досліджуємо будову атома

• Субатомні частики: протони, нейтрони, електрони
• Протонне, нейтронне, нуклонне / масове числа
• Внесок видатного українця Дмитра Іваненка у дослідження будови атома
• Будова ядра й електронної оболонки атома
• Поняття про атомну орбіталь, енергетичний рівень і підрівень
• Електронна формула атома та її запис
• Взаємозв’язок властивостей елементів і будови електронної оболонки атома
• Фізичний зміст і значення періодичного закону
• Періодична система хімічних елементів і будова атомів
• Довга і коротка форми періодичної таблиці
• Характеристика хімічного елемента за місцем у періодичній системі та будовою атома
• Діагностування й самооцінювання власних результатів навчання
§ 27. Субатомні частинки
• Опиши будову атома Карбону за моделлю (мал. 38).
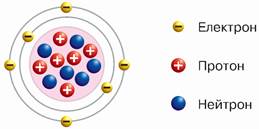
Мал. 38. Модель атома Карбону
• У ядрі атома є 16 протонів. Як дізнатися, який це хімічний елемент? Скільки електронів у електронній оболонці його атома?
Опрацюй. Зрозумій. Використай
Слово «атом» перекладається українською як «неподільний». Тривалий час його вважали неподільною структурною частинкою речовини. Чи дійсно це так? Експериментальні дослідження, здійснені вченими на початку XXI століття, спростували цю думку. Доведено, що атом складається з протонів, електронів і нейтронів, що називають субатомними частинками.
У 1897 році англійський учений Джозеф Джон То́мсон (1856-1940) відкрив електрон. Абсолютна маса електрона в тисячі разів менша, ніж маса найлегшого атома Гідрогену. З наведеної інформації стає зрозумілим походження назви «субатомні» — менші за атом (префікс «суб-» походить із латинської мови та означає «нижче», «менше»).
Завдання 1. Наведи власні пояснення слів субмолекулярний, субтропічний. Порівняй їх з означеннями в довідниках чи словниках термінів.
Електрон — негативно заряджена субатомна частинка, заряд якої найменший з усіх відомих зарядів. Умовно його прийнято за —1.
У 1919 році Ернест Резерфо́рд відкрив протон — позитивно заряджену субатомну частинку в складі ядра атома. Чисельне значення заряду протона виявилось таким самим, як у електрона, відтак заряд протона умовно дорівнює +1.
У 1932 році наявність нейтронів у ядрі атома експериментально довів англійський фізик Джеймс Чедвік (1891-1974). Цього ж року видатний фізик з України Дмитро Дмитрович Іваненко першим запропонував протонно-нейтрону модель атомного ядра. За розробленою ним моделлю ці субатомні частинки заряду не мають, а їх маса приблизно однакова з масою протона.
Для кожної субатомної частинки використовують певні позначення: протон — р або 1+1р, нейтрон — n або 10n, електрон — е або 0-1е. Субатомні частинки мають надзвичайно малу масу: маса протона приблизно дорівнює масі нейтрона, маса електрона в 1836 разів менша від маси протона. В науці масу протона і масу нейтрона прийнято за 1, маса електрона дорівнює 1/1836. Ядро має позитивний заряд і дуже малі розміри порівняно з атомом. В ядрі зосереджена основна маса атома. Електронна оболонка атома складається з негативно заряджених електронів. Числові значення заряду ядра й електронної оболонки атома однакові.
Завдання 2. Використовуючи наведену в таблиці 20 інформацію, склади схему «Будова атома».
Таблиця 20
|
Субатомна частинка |
Розміщення в атомі |
Заряд (в одиницях елементарного заряду) |
Маса |
|
|
відносна (а. о. м.) |
абсолютна (кг) |
|||
|
Протон, 1+1р |
ядро |
+1 |
1 |
1,627 • 10-27 |
|
Нейтрон, 10n |
ядро |
0 |
1 |
1,625 • 10-27 |
|
Електрон, 0-1e |
електронна оболонка |
-1 |
1/1836 |
9,109 • 10-31 |
Електрони, протони, нейтрони — субатомні частинки.
Електрони мають негативний заряд, протони — позитивний, нейтрони — незаряджені частинки. В атомі кількість позитивно заряджених протонів дорівнює кількості негативно заряджених електронів, тому атом електронейтральний.
ПЛІЧ-О-ПЛІЧ
Завдання 1. Скористайтеся доступними джерелами інформації і дослідіть ключові історичні події, пов’язані з відкриттям будови атома.
Завдання 2. Створіть стрічку часу, яка включатиме важливі події у з’ясуванні будови атома. Для кожної події вкажіть:
- дату або період часу;
- ім’я дослідника;
- короткий опис події (відкриття, експерименту);
- внесок події у розуміння будови атома.
Зверніть увагу, що всі події мають бути представлені у хронологічному порядку.
Завдання 3. Додайте зображення або ілюстрації, наприклад портрети вчених, схеми моделей атома чи цікаві факти про науковців.
Завдання 4. Сформулюйте висновок, як і під впливом чого змінювались уявлення про будову атома.
ПРОТОННЕ, НЕЙТРОННЕ, НУКЛОННЕ / МАСОВЕ ЧИСЛА. Протонним числом (Z) називають кількість протонів у ядрі атома. Воно збігається з порядковим номером хімічного елемента у періодичній таблиці.
Нейтронне число (N) — кількість нейтронів у ядрі атома.
Нуклонне, або масове число (А) — сума протонного і нейтронного чисел: А = Z + N.
Для обчислення нейтронного числа необхідно від нуклонного числа відняти протонне: N = А - Z.
Завдання 3. Скористайся періодичною таблицею як довідковою і визнач протонне, нейтронне й нуклонне / масове числа Алюмінію та Аргону.
Ядра атомів одного й того самого хімічного елемента мають однакові протонні числа, проте можуть відрізнятись нейтронними числами. Наприклад, у природі існують два різновиди атомів Бору — з нуклонними числами 10 і 11, проте заряд ядра в обох однаковий і дорівнює +5. В ядрі атома з нуклонним числом 10 міститься 5 нейтронів (10 - 5 = 5), нейтронне число (N) дорівнює 5, а в ядрі атома з нуклонним числом 11 міститься 6 нейтронів (11 - 5 = 6), тобто нейтронне число (N) дорівнює 6 (мал. 39).
Щоб відрізняти атоми одного хімічного елемента з різними нуклонними числами, у науковий обіг введено поняття нуклід (у перекладі з латинської мови nucleus означає «ядро»). Так називають різновид атомів з певним нуклонним і протонним числом.
Нукліди — це атоми одного й того самого хімічного елемента з однаковою кількістю протонів і різною кількістю нейтронів, а отже, з різними нуклонними / масовими числами.
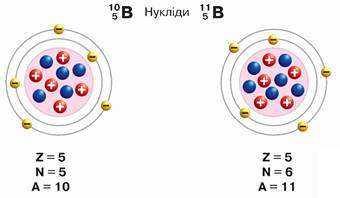
Мал. 39. Моделі нуклідів Брому
Розглянутий вище приклад ілюструє існування двох нуклідів Бору. Для їх позначення застосовують символи нуклідів: 105В і 115В.
Можуть також використовуватися записи без зазначення протонного числа: 10В і 11В або В-10, В-11.
Аналогічно записують нукліди інших хімічних елементів.
Завдання 4. Обчисли, скільки нейтронів містить кожен нуклід Оксигену з нуклонними числами 32, 33 і 34. Запиши символи нуклідів Оксигену.
Нукліди одного хімічного елемента називають ізотопами. Вони мають однакову кількість протонів і різну кількість нейтронів, а тому відрізняються масовими / нуклонними числами.
Ізотопи поділяють на природні і штучні. А ще ізотопи бувають стабільні та нестабільні (радіоактивні).
Завдання 5. Поміркуй, що можуть означати ці терміни. За потреби звернись до додаткових інформаційних джерел. Прикладом природних стабільних ізотопів Карбону є нукліди 12С і 13С (або С-12 і С-13). У природі в невеликих кількостях існує нестабільний (радіоактивний) нуклід Карбону 14С, його одержують також штучно.
Ізотоп у перекладі з грецької означає «однакове місце». Таким місцем є клітинка періодичної таблиці. Наприклад, для десяти природних ізотопів Стануму Sn — це клітинка під номером 50. У клітинках періодичної таблиці для кожного елемента вказано середнє значення відносної атомної маси всіх його природних ізотопів. Тому, на відміну від нуклонних / масових чисел, вона виражена дробовим, а не цілим числом.
ХІМІЧНА СКАРБНИЦЯ

Дмитро Дмитрович Іваненко (1904-1994) — український фізик, який зробив вагомий внесок у розвиток ядерної фізики, теорії поля та теорії гравітації. Присвятивши життя науці, вже у 27 років молодий учений став професором.
Світове визнання Д. Д. Іваненко здобув тим, що запропонував протонно-нейтронну модель атомного ядра: на основі експериментальних даних він висловив ідею, що ядро складається з протонів і нейтронів.
Наукова спадщина Дмитра Дмитровича Іваненка налічує понад 400 робіт у різних сферах: математична фізика, біологія, філософія, геологія, історія науки.
Медіапошук
Скористайся доступними джерелами інформації та напиши есе на тему: «Оцінка лауреатами Нобелівської премії наукового внеску Дмитра Дмитровича Іваненка». У своєму есе зазнач, які досягнення Іваненка отримали найбільше визнання та які відгуки на його роботу залишили лауреати Нобелівської премії. Зверни увагу, що праці видатного українця вплинули на відкриття інших фізиків, що здобули міжнародне визнання, як-от Лев Ланда́у, Енріко Фермі.
ТОБІ ДО СНАГИ
1. Які частинки називають субатомними? Наведи приклади заряджених субатомних частинок.
2. Чому атом не має заряду?
3. Запиши протонне і нейтронне числа для нуклідів Сульфуру з нуклонними числами 32 і 34.
4. Обери правильні твердження і виправ помилки у неправильних:
- а) нейтрон має позитивний заряд;
- б) заряд електрона дорівнює -1;
- в) величина заряду ядра атома дорівнює сумі протонів і нейтронів;
- г) кількість електронів у атомі дорівнює кількості протонів у ядрі.
5. Скільки протонів й електронів мають нукліди Феруму 5426Fe, 5626Fe, 5826Fe?
6. Знана українська дитяча письменниця Оксана Дмитрівна Іваненко (1906-1997) є сестрою Дмитра Дмитровича Іваненка — дослідника субатомних частинок.

Фото з юнацьких років Оксани і Дмитра Іваненків
Оксана Дмитрівна відома своїми казками і прозовими творами, зокрема романами «Тарас Шевченко» і «Марія» (про Марка Вовчка).
Чи відомі тобі твори Оксани Іваненко? Дізнайся більше про доробок письменниці і, спираючись на її творчий підхід, спробуй написати казку чи оповідання, героями яких будуть хімічні елементи або субатомні частинки. Презентуй свій твір у самостійно дібраний спосіб учнівству класу.
