Фізика. Рівень стандарту. Повторне видання. 11 клас. Бар’яхтар
Розділ IV. Атомна та ядерна фізика
§ 36. Дослід Е. Резерфорда. Постулати Н. Бора. Енергетичні рівні атома

30 квітня 1897 р. на засіданні Лондонського королівського товариства англійський фізик Джозеф Джон Томсон (1856-1940) доповів про експериментальне підтвердження існування субатомних частинок, а саме електронів, гіпотеза про існування яких була висунута фізиками за 40 років до цього. Дата доповіді Томсона вважається «днем народження» електрона. Можна сказати, що саме в цей день фізики остаточно переконалися в тому, що атом має складну будову. Тож яку будову має атом?
1. Як з'явилась ядерна модель атома
Саме Дж. Томсон у 1903 р. запропонував одну з перших моделей будови атома. Він припустив, що атом має форму кулі, по всьому об’єму якої рівномірно розподілений позитивний заряд, а негативно заряджені електрони вкраплені в кулю (рис. 36.1); сумарний заряд електронів дорівнює заряду кулі, тому атом є електрично нейтральним.
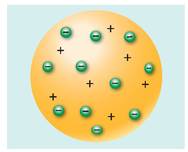
Рис. 36.1. Модель атома Томсона («пудинг із родзинками»)
• Як ви вважаєте, чому модель атома, запропонована Дж. Томсоном, отримала назву «пудинг із родзинками»?
Подальший прогрес у дослідженнях внутрішньої структури атома пов’язаний з ім’ям англійського фізика Ернеста Резерфорда (1871-1937). У дослідах, проведених під його керівництвом у 1908-1911 рр., вивчалося розсіювання α-частинок ядрами атомів золота.
Для дослідів учені використали α-радіоактивну речовину, яку розташували у свинцевому контейнері з вузьким отвором. Пучок α-частинок із контейнера спрямовувався на тонку золоту фольгу, а далі потрапляв в екран, покритий шаром кристалів цинк сульфіду (рис. 36.2). Якщо в такий екран влучала α-частинка, то в місці її влучання відбувався слабкий спалах світла. Учені спостерігали спалахи за допомогою мікроскопа та реєстрували місця влучання α-частинок в екран.
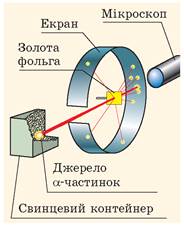
Рис. 36.2. Схема досліду з розсіювання α-частинок (дослід Резерфорда)
У результаті дослідів було виявлено: 1) переважна більшість α-частинок проходить крізь золоту фольгу, не змінюючи напрямку свого руху; 2) деякі з α-частинок відхиляються від початкової траєкторії; 3) приблизно одна з 20 000 α-частинок відскакує від фольги, начебто натикаючись на якусь перешкоду (рис. 36.3).
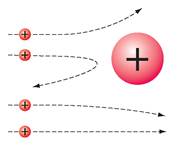
Рис. 36.3. Траєкторії α-частинок, що пролітають поряд із ядром атома золота
Зрозуміло, що Е. Резерфорд не міг бачити внутрішню структуру атома, тому він залучив логіку.
Якщо позитивний заряд і маса рівномірно розподілені по всьому об’єму атома (так вважав Дж. Томсон), то всі α-частинки повинні пролетіти крізь фольгу практично не відхиляючись (маленькі електрони не можуть зупинити досить важкі й швидкі α-частинки — ядра атома гелію, що рухаються зі швидкістю 10 000 км/с).
Якщо ж позитивний заряд і маса зосереджені всередині атома — у невеликому порівняно з атомом об’єкті, — то, зіштовхнувшись із ним, позитивно заряджена α-частинка може відскочити назад, а ті α-частинки, які пролітають близько до цього об’єкта, можуть відхилитися внаслідок електричного відштовхування.
Очевидно, що результатам експерименту відповідає саме друге припущення. У 1911 р., після дослідів із розсіяння α-частинок, Резерфорд запропонував планетарну (ядерну) модель будови атома: атом складається з позитивно зарядженого ядра, в якому зосереджена мало не вся маса атома; біля ядра по певних орбітах обертаються електрони (рис. 36.4).
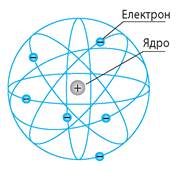
Рис. 36.4. Планетарна модель будови атома, запропонована Е. Резерфордом. Учений також розрахував розмір ядра: воно виявилося дуже малим — порядку 10-15 м, що в 100 000 разів менше, ніж розмір атома (10-10 м).
Планетарна модель атома, блискуче пояснивши результати експериментів із розсіювання α-частинок, разом із тим суперечила законам класичної електродинаміки.
Річ у тім, що рух планетарною орбітою є рухом із прискоренням (доцентровим), а відповідно до теорії Дж. Максвелла прискорений рух зарядженої частинки має супроводжуватися випромінюванням електромагнітних хвиль. Таким чином, електрон в атомі мав би випромінювати електромагнітні хвилі, а отже, втрачати енергію. А наслідками цього були б зменшення швидкості руху електрона та його падіння на атомне ядро (рис. 36.5). Проте атом є дуже стійким...
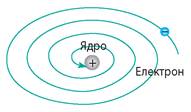
Рис. 36.5. Якби електрон рухався навколо ядра планетарною орбітою, то відповідно до законів класичної фізики він мав би за 10-8 с упасти на ядро, а власне атом припинив би своє існування
2. Постулати Н. Бора
Модифікацію планетарної моделі запропонував у 1913 р. данський фізик Нільс Бор (1885-1962), який був упевнений, що розглядати будову атома слід із точки зору квантових уявлень. Бор припустив існування особливих станів атомів і сформулював два постулати. Наведемо постулати Бора в сучасному формулюванні.
Перший постулат Н. Бора (про стаціонарні стани):
Атомна система може перебувати тільки в особливих стаціонарних (квантових) енергетичних станах, кожному з яких відповідає певне значення енергії; перебуваючи в стаціонарному стані, атом не випромінює енергію.
Другий постулат Н. Бора (про квантові стрибки):
При переході з одного стаціонарного енергетичного стану в інший атом випромінює або поглинає квант електромагнітної енергії:
hv = |Ek - Еm|,
де hν — енергія кванта; Ek — енергія початкового стану атома; Еm — енергія стану, в який перейшов атом.
Випромінювання кванта енергії (фотона) відбувається внаслідок переходу атома зі стану з більшою енергією у стан із меншою енергією (Ek > Еm); у результаті поглинання кванта атом переходить зі стану з меншою енергією у стан із більшою енергією (Ek < Еm) (рис. 36.6).
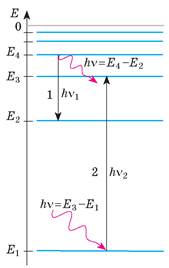
Рис. 36.6. Схема переходів атома з одного енергетичного стану в інший (переходи показано стрілками): у разі переходу на нижчий енергетичний рівень атом випромінює квант електромагнітної енергії (перехід 1), а поглинувши квант, атом стрибком переходить на вищий енергетичний рівень (перехід 2)
• Атом водню перейшов зі стану з енергією -13,6 еВ у стан з енергією -3,4 еВ. У цьому випадку атом поглинув фотон чи випромінив?
Для атома дійсно стійким є тільки стаціонарний. стан із найнижчим рівнем енергії — основний стан, у якому атом може перебувати нескінченно довго. Щойно атом буде переведено у стан із вищим рівнем енергії, тобто щойно атом поглине фотон певної частоти, як цей атом довільно перейде в основний стан із випромінюванням фотона такої самої частоти або кількох фотонів менших частот. Саме тому всі стаціонарні стани атома, крім основного, називають збудженими станами.
Зверніть увагу!
• Енергія будь-якого стаціонарного стану атома є від’ємною, оскільки зумовлена взаємодією електронної хмари і ядра атома, що мають заряди протилежних знаків.
• Енергію енергетичних станів атомів зазвичай подають в електрон-вольтах (еВ), тому, розв’язуючи задачі, сталу Планка краще брати в електрон-вольт-секундах:
h ≈ 4,14 • 10-15 еВ • с
Зверніть увагу! Стаціонарний стан атома означає, що його електрони певним (визначеним) чином локалізовані в просторі: у Н. Бора йшлося про орбіти електрона, зараз ми говоримо про орбіталі. При квантовому переході атома з одного енергетичного стану в інший змінюється форма електронної хмари.
Хвилі чи частинки? І не хвилі, і не частинки!

«Речовина і світло одночасно мають властивості хвиль і частинок, однак у цілому це не хвилі, й не частинки, і не суміш того й іншого. Наші механічні поняття не спроможні повністю охопити реальність, для цього недостатньо реальних образів».
Сергій Вавилов (1891-1951)
3. Фізичні основи квантової механіки
Формулюючи свої постулати, Н. Бор, як і Е. Резерфорд, спирався на уявлення, що електрон усередині атома поводиться як частинка, що рухається певною орбітою. І в цьому була його помилка. Кількісна теорія, побудована Бором, виявилася недостатньою, щоб пояснити випромінювання складних атомів і випромінювання молекул, — учений зміг побудувати лише теорію випромінювання атома водню.
Річ у тім, що поведінка електрона всередині атома скоріше нагадує хвилю. «Але ж електрон — це частинка», — скажете ви і будете й праві, й не праві, адже електрон, як і світло, одночасно має властивості хвилі й частинки.
У 1924 р. французький фізик Луї де Бройль (1892-1987) висунув гіпотезу, згідно з якою корпускулярно-хвильовий дуалізм є характерним не лише для фотонів, а й для будь-яких інших мікрочастинок.
Корпускулярно-хвильовий дуалізм — універсальна властивість матеріальних об'єктів, яка полягає в тому, що в поведінці того самого об'єкта можуть виявлятись і корпускулярні, і хвильові риси.
Уявлення про корпускулярно-хвильовий дуалізм частинок лежить в основі квантової механіки, яка є одним із основних напрямів сучасної фізики.

Довжина хвилі де Бройля для всіх частинок виявляється дуже малою. Наприклад, для електронів, розігнаних до швидкості 7,3 • 106 м/с, вона дорівнює 1 • 10-10 м (розмір атома), а для нейтронів, що вилітають зі швидкістю 4·• 106 м/с з ядра атома урану під час поділу ядра, — лише 1 • 10-13 м.
Разом із тим зараз експериментально виявлено хвильові властивості не тільки електронів та інших елементарних частинок (рис. 36.7), але й атомів і молекул.
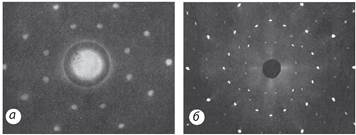
Рис. 36.7. Дифракція нейтронів (а) і рентгенівських променів (б) на монокристалі NaCI, який виконує функцію дифракційної ґратки
Квантова механіка, на відміну від класичної, використовує інший метод опису стану системи. У будь-якій задачі класичної механіки матеріальна точка (або тіло) має визначені координати, які характеризують її положення в просторі, та визначену швидкість (або імпульс). У квантовій механіці й координата, й імпульс одночасно визначаються лише з деякою точністю (Δx — невизначеність координати; Δр — невизначеність імпульсу), тобто можна знайти лише ймовірність виявлення об’єкта в певній ділянці простору, ймовірність наявності в об’єкта певного імпульсу.
Підбиваємо підсумки
• Дослідження, проведені фізиками в XIX ст., довели атомарну структуру речовини й підтвердили, що атом має складну будову.
• Експерименти під керівництвом Е. Резерфорда дозволили створити планетарну модель атома.
• Розвитком планетарної моделі атома стали постулати Бора, згідно з якими атоми можуть перебувати тільки в певних стаціонарних станах. У стаціонарному стані атом не випромінює електромагнітні хвилі. Випромінювання/поглинання електромагнітних хвиль (чітко визначеної частоти) відбувається тільки при переході атома з одного стаціонарного стану в інший.

Контрольні запитання
1. Опишіть модель атома Дж. Томсона. 2. Опишіть дослід під керівництвом Е. Резерфорда із розсіювання α-частинок ядрами атомів золота. Яких висновків дійшов Резерфорд на підставі результатів цього досліду? 3. У чому розбіжність між моделями атомів, запропонованими Дж. Томсоном і Е. Резерфордом? 4. У чому недосконалість планетарної моделі атома? 5. Сформулюйте постулати Н. Бора. 6. У чому сутність корпускулярно-хвильового дуалізму?
Вправа № 36
1. На схемі енергетичних рівнів деякого атома (рис. 1) подано переходи цього атома з одного енергетичного стану в інший. Під час яких переходів атом випромінює фотон? поглинає фотон?
2. Під час якого переходу атома (див. рис. 1) частота випроміненого або поглиненого ним фотона є найбільшою? Під час якого переходу є більшою довжина хвилі?
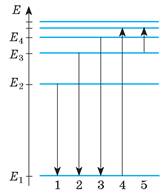
Рис. 1
3. Під час переходу атомів ртуті в основний стан випромінюються фотони з енергією 4,5 еВ. Якою є довжина хвилі випромінювання?
4. На схемі енергетичних рівнів деякого атома (рис. 2) подано переходи цього атома з одного енергетичного стану в інший. Визначте, фотон якої енергії поглине атом, якщо перейде: а) зі стану Е1, у стан Е2; б) зі стану Е1 у стан Е4. Відомо, що ν13 = 6 • 1014 Гц, ν24 = 4 • 1014 Гц, ν32 = 3 • 1014 Гц.
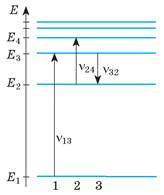
Рис. 2
5. У Великому адронному колайдері протони сягають швидкості, яка лише на 3 м/с менша від швидкості поширення світла у вакуумі. Визначте довжину хвилі де Бройля для цих протонів. Маса протона 1,7 • 10-27 кг.
6. Дізнайтесь, чому на рисунку на початку параграфа зображено трубку Крукса.
