Хімія. Повторне видання. 9 клас. Григорович
Цей підручник можна завантажити у PDF форматі на сайті тут.
§ 23. Метан — найпростіший вуглеводень
Пригадайте:
- складання електронно-графічних формул молекул (за § 2);
- порівняти густину газів можна, обчисливши відносну густину газу, що дорівнює відношенню молекулярних мас газів (Додаток 1).
Молекулярна й структурна формули метану
Із попереднього параграфа ви вже дізналися, що найпростішими органічними речовинами є вуглеводні — речовини, які складаються з атомів тільки двох елементів: Карбону й Гідрогену. Серед вуглеводнів найпростішими сполуками є насичені вуглеводні, або алкани.
Молекулярна формула метану — СН4. У цій молекулі чотири атоми Гідрогену сполучені ковалентними зв’язками з атомом Карбону, і структурна формула метану має вигляд:

У Карбону й Гідрогену близькі значення електронегативностей (2,55 та 2,20 відповідно). Тому зв’язок між ними є ковалентним неполярним. Молекула метану також неполярна.
Будова молекули метану. Основний і збуджений стани атома Карбону
У молекулі метану наявні чотири зв’язки С-Н — це ковалентні зв’язки, для реалізації яких необхідно утворення чотирьох спільних електронних пар:

Пригадайте, що у звичайному (основному) стані на зовнішньому енергетичному рівні атома Карбону міститься чотири електрони: одна пара на s-орбіталі та два неспарені електрони на р-орбіталях.
У такому стані атом Карбону може утворити тільки два ковалентні зв’язки. Але для утворення чотирьох зв’язків на зовнішньому рівні має бути чотири неспарені електрони. Для цього атом Карбону поглинає невелику кількість енергії та переходить у збуджений стан, в якому один електрон із s-орбіталі переходить на вільну р-орбіталь.

Мал. 23.1. В атомі Карбону в основному стані s-орбіталь і три р-орбіталі розташовуються так, що ядро атома збігається із центром кожної орбіталі. За такого розташування s-орбіталь недоступна для перекривання

Мал. 23.2. Змінені орбіталі зовнішнього енергетичного рівня (а) та їх розташування в атомі Карбону в збудженому стані (б)

Але навіть за умови такого переходу одного електрона одна s-орбіталь і три р-орбіталі зовнішнього рівня не можуть утворити чотири зв’язки, оскільки s-орбіталь просторово недоступна для перекривання з орбіталями інших атомів (мал. 23.1). Саме тому, коли атом Карбону переходить у збуджений стан, усі чотири орбіталі зовнішнього енергетичного рівня набувають однакової енергії, а отже, і форми (несиметричної об’ємної вісімки) (мал. 23.2, а) і орієнтуються вже по-іншому (мал. 23.2, б): вони спрямовані до вершин правильної трикутної піраміди (тетраедра). За такої форми та спрямованості всі орбіталі в збудженому стані атома Карбону без обмежень можуть перекриватися з орбіталями інших атомів (мал. 23.3).
Під час утворення хімічних зв’язків між атомами Карбону й Гідрогену ці зв’язки також спрямовуються до вершин трикутної піраміди під кутом 109,5°, тому молекули метану мають форму тетраедра (мал. 23.4).

Мал. 23.3. Перекривання орбіталей збудженого атома Карбону із s-орбіталями атомів Гідрогену в молекулі метану

Мал. 23.4. Моделі молекули метану: а — кульова; б — кулестрижнева
Зміну форми й спрямованості атомних орбіталей під час переходу атомів у збуджений стан називають гібридизацією, а орбіталі, що зазнали зміни, називають гібридизованими. Під час утворення молекули метану змін зазнають одна s-орбіталь і три р-орбіталі, тому такий стан атома Карбону називають sр3-гібридизованим (див. малюнок).
Три однакові р-орбіталі в атомі Карбону в основному стані мають бути розташовані таким чином, щоб бути максимально віддаленими одна від одної. Саме тому р-орбіталі розташовані по взаємно перпендикулярних осях (мал. 23.1). У збудженому стані однакових (гібридизованих) орбіталей уже чотири, і вони також мають бути максимально віддаленими одна від одної. Саме цим і пояснюється тетраедрична спрямованість sр3-гібридизованих орбіталей. Явище гібридизації пояснює форму як органічних, так і неорганічних молекул, але це ви розглядатимете під час поглибленого вивчення хімії.

Фізичні властивості метану та поширеність у природі
Метан — за звичайних умов безбарвний газ без запаху; густина за 0 °С дорівнює 0,7168 кг/м3, нерозчинний у воді (0,02 г метану в 1 кг води за 25 °С), у разі сильного охолодження перетворюється на летку рідину (tкип. = -161,6 °С), а в разі подальшого охолодження — на безбарвні кристали (tпл. = -182,5 °С).
За концентрації в повітрі від 4,4 до 17 % метан вибухає. Метан є основним компонентом природного газу, яким ми користуємося в побуті, і тому витік газу може спричинити серйозні наслідки (мал. 23.5). Через відсутність в метану запаху виявити його витік було б неможливо, тому до природного газу ще в момент видобутку додають спеціальні речовини із запахом (одоранти). Зазвичай це органічні речовини класу меркаптанів, що мають характерний запах тухлого м’яса.

Мал. 23.5. Наслідки вибуху природного газу в багатоповерховому житловому будинку, 13 жовтня 2007 року, м. Дніпро
Метан нетоксичний і в малих концентраціях безпечний для людини, але за значного вмісту метану в повітрі (25-30 %) людина може знепритомніти й померти, оскільки метан не підтримує дихання.
Метан — один із парникових газів, оскільки він виявляє парниковий ефект, причому навіть сильніший за вуглекислий газ у 20-25 разів. Останніми роками концентрація метану в повітрі суттєво збільшується через інтенсивний розвиток тваринництва: кожна корова за добу випускає близько 300 л метану, а світове поголів’я корів налічує понад 1,5 млн, не враховуючи іншу велику рогату худобу.
Метан — поширена в природі речовина. Його вміст у природному газі становить 77-99 %, у супутньому нафтовому газі — 31-90 %. Також метан міститься у складі рудничного (того, що виділяється в рудниках) та болотного (того, що виділяється на болотах) газів.
В Україні запаси метану у вигляді природного газу оцінюють приблизно в 1,5 трлн м3 (28-ме місце серед усіх країн світу). Найбільші родовища газу в Україні зосереджені в Дніпровсько-Донецькому нафтогазоносному регіоні та в Передкарпатському родовищі. Значні родовища природного газу є на рівнинній частині Кримського півострова та в Чорноморському й Азовському шельфах. Також, за думкою багатьох фахівців, Україна має великі перспективи добування природного газу світового масштабу в північній частині Чорноморського шельфу, де, можливо, зосереджене найбільше родовище природного газу під дном Чорного моря.
У великих обсягах метан транспортують трубопроводами. Також метан можна зберігати за підвищеного тиску в спеціальних сталевих балонах, забарвлених у червоний колір (мал. 23.6).

Мал. 23.6. Сталеві балони з метаном забарвлюють у червоний колір
Суттєва кількість метану існує на Землі у вигляді так званих газогідратів (продуктів сполучення з водою). Такі сполуки існують лише за умови низької температури та високого тиску, тому трапляються переважно в північних морях і залягають на глибині близько 1 км. Запаси такого метану оцінюють у 100 разів більшими, ніж запаси всіх розвіданих на сьогодні родовищ природного газу.
• Вибір меркаптану для надання запаху метану не випадковий: нюх людини може сприйняти запах меркаптану, навіть якщо в 1 л повітря його буде лише 10-16 моль. У такій концентрації навіть собака не здатний відчути його запах.
• В Україні газове освітлення вулиць (із використанням метану) уперше було запроваджено у Львові 1858 року, а потім з'явилося в Одесі, Харкові, Києві та Чернівцях. Пізніше в цих містах газ почали використовувати як паливо.
Газогідрати є клатратними сполуками (від латин. clathratus — той, що закритий ґратками, посаджений у клітку), або сполуками включення. Клатратними називають сполуки, в яких маленькі молекули, такі як у метану, розміщені в порожнинах між молекулами рідкої води (як зображено на малюнку) і фактично є газовими гідратами. Такі сполуки характерні для багатьох газуватих речовин, зокрема метану, але вони стійкі тільки за умов високого тиску та низької температури. У разі потрапляння гідрату метану у звичайні умови він розкладається на газуватий метан і рідку воду. Один об'єм гідрату метану може виділити 160-180 об'ємів чистого газу.
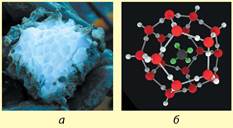
Зовнішній вигляд клатрату метану (а) та його будова (б) (жовтими лініями позначено водневі зв'язки)
Ключова ідея
Вуглеводні — найпростіші органічні речовини, що складаються з атомів Карбону та Гідрогену. Метан — найпростіший вуглеводень.
Контрольні запитання
- 261. Напишіть структурну й електронну формули метану. Назвіть тип зв'язку в метані.
- 262. Чим відрізняються основний та збуджений стани атомів Карбону? Як це пов'язано з можливістю утворення молекули метану та її формою?
- 263. Опишіть фізичні властивості метану.
- 264. Для чого в природний газ додають речовини із сильним запахом?
Завдання для засвоєння матеріалу
265. Обчисліть, у скільки разів густина метану більша (менша) за повітря.
266. Використовуючи інформацію параграфа, обчисліть масову частку метану в його насиченому за 25 °С розчині у воді.
267. За температури 0 °С розчинність метану у воді становить 0,04 г на 1 кг води. Обчисліть об'єм метану, що можна виділити з насиченого за такої температури розчину масою 1000 кг.
268. Обчисліть мінімальний об'єм метану, що має витекти з побутової газової печі, щоб повітря на кухні стало вибухонебезпечним. Прийміть, що площа кухні становить 10 м2, висота стелі — 2,5 м, а тиск на кухні не змінюється. Інші дані знайдіть у тексті параграфа. (Пам'ятайте, що витік будь-якої кількості газу є вкрай небезпечною ситуацією!)
269. 2015 року споживання природного газу в Україні становило близько 34 млрд м3 на рік. Знайдіть у тексті параграфа необхідну інформацію та обчисліть, на скільки років Україні вистачить власних розвіданих запасів природного газу за умови споживання на такому самому рівні.
