Підручник з Хімії. 10 клас. Величко - Нова програма
Цей підручник можна завантажити у PDF форматі на сайті тут.
Вуглеводи
Нові поняття й терміни:
моно-, ди-, оліго-, полісахариди, перспективні формули, рибоза, дезоксирибоза, оптична ізомерія, штучний шовк.
Вуглеводи — найпоширеніший клас природних органічних сполук і важливий компонент організмів, джерело їхньої енергії та будівельний матеріал. Ви вже знаєте про походження назви вуглеводи, хімічний склад і деякі властивості глюкози, сахарози, крохмалю, целюлози. Тепер розглянемо ці сполуки докладніше.
Передусім пригадайте, як у природі утворюється глюкоза. Процес фотосинтезу відбувається в рослинних клітинах під упливом сонячної енергії та за участю зеленого пігменту хлорофілу, що вбирає цю енергію. Загалом процес фотосинтезу виражають хімічним рівнянням:

У рослинах із глюкози утворюються сахароза, крохмаль, целюлоза.
Класифікація вуглеводів. Залежно від складу вуглеводи поділяють на такі групи:
моносахариди, або прості вуглеводи (до них належать глюкоза, фруктоза, рибоза). Це поліфункціональні сполуки, гідроксіальдегіди або гідроксикетони, що містять декілька гідроксильних груп та альдегідну або карбонільну групу;
олігосахариди можна розглядати як продукти сполучення декількох молекул моносахаридів. Найважливіші з них — дисахариди (сахароза, мальтоза, лактоза);
полісахариди — полімерні сполуки, продукти конденсації великої кількості молекул моносахаридів (крохмаль, целюлоза).
Серед моносахаридів розрізняють тетрози, пентози, гексози, молекули яких складаються відповідно з чотирьох, п’яти, шести атомів Карбону. Глюкоза й фруктоза належать до гексоз, рибоза — до пентоз.
Належність сполук до класу вуглеводів підкреслюється в їхній назві закінченням -оза.
§ 34. ГЛЮКОЗА
Склад і будова молекули. Молекулярна формула глюкози С6Н12О6.
У кристалічному стані глюкоза існує у вигляді шестичленних циклів, причому п’ять кутів займають атоми Карбону, а один кут — атом Оксигену. Структуру глюкози прийнято зображати за допомогою так званих перспективних формул:
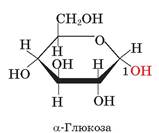

У молекулі глюкози містяться п’ять гідроксильних груп. Спосіб розміщення гідроксильної групи біля першого атома Карбону зумовлює існування двох ізомерів глюкози: а- і β-форм. В а-глюкозі гідроксильна група розміщена під площиною циклу, а в β-глюкозі — над цією площиною.
Проте це не єдині відомі форми глюкози. Виявляється, що у водних розчинах разом із циклічними існує в невеликій кількості відкрита форма глюкози. Під упливом полярних молекул води відбувається гідратація глюкози, і певна частина гідратованих молекул переходить у відкриту форму:

Схему утворення циклічної форми глюкози наведено на мал. 120.

Мал. 120. Схема утворення циклічної форми глюкози
У рівняннях хімічних реакцій глюкозу у відкритій формі прийнято зображати у спрощеному вигляді: СН2ОH(СНОН)4СНО. Відкрита форма характеризується наявністю в молекулі альдегідної групи.
Розрив циклу та його утворення — процес динамічної рівноваги: щойно розкрившись, наступної миті цикл знову замикається, і при цьому приєднання спиртової групи до альдегідної можливе з обох боків площини, тобто може утворитися а- або β-форма глюкози.
Під час кристалізації співвідношення між а- і β-формами зберігається, а відкрита форма зникає.
Фізичні властивості. Глюкоза — безбарвна кристалічна речовина, добре розчинна у воді, солодка на смак (пригадайте походження терміна глюкоза). У вільному стані міститься в багатьох фруктах, зокрема у винограді (звідси походить інша назва глюкози — виноградний цукор), меду, є вона й у корінні, листках і квітах рослин, у крові людини й тварин (близько 0,1 %).
Виноградний цукор — це чиста а-глюкоза, перекристалізацією її з піридину можна добути β-глюкозу. Як ізомери а- і β-глюкоза мають різні фізичні властивості, зокрема різні температури плавлення.
Хімічні властивості. Рівняння реакцій глюкози наведено на с. 190. Наявність функціональних гідроксильних груп, а у відкритій формі ще й альдегідної групи визначає реакції глюкози. За альдегідною групою — це реакції окиснення й відновлення.
Унаслідок повного окиснення глюкози сильними окисниками вона перетворюється на вуглекислий газ і воду.
У результаті реакції з амоніаковим розчином аргентум(І) оксиду (реакція «срібного дзеркала») альдегідна група окиснюється до карбоксильної й утворюється глюконова кислота.
Як альдегід глюкоза окиснюється і в результаті нагрівання з купрум(ІІ) гідроксидом.
Складіть рівняння цієї реакції.
Хоча відкритої форми глюкози у водному розчині дуже мало, дослід засвідчує, що ця реакція відбувається до кінця. Як узгодити ці факти? Оскільки з трьох форм глюкози для реакції затрачається лише одна, то хімічна рівновага між різними формами зміщується в бік утворення відкритої (альдегідної) форми, компенсуючи її затрачання аж до повного перетворення глюкози на глюконову кислоту.
Реакції глюкози
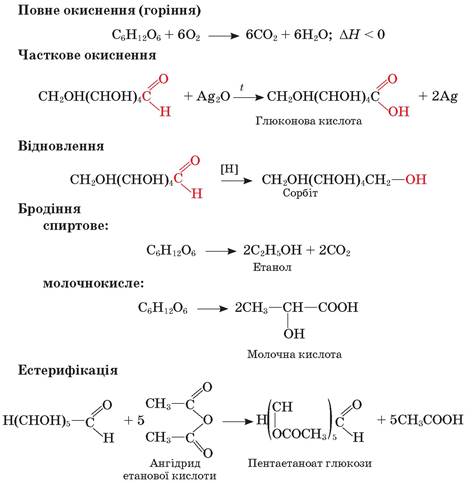
Енергійніший окисник (наприклад, концентрована нітратна кислота) окиснює не лише альдегідну, а й первинну спиртову групу відкритої форми глюкози. У результаті утворюється дикарбонова глюкарова кислота:

Унаслідок відновлення альдегідної групи до спиртової утворюється шестиатомний спирт сорбіт. Ця сполука є замінником цукру в дієті хворих на діабет, а також вихідною речовиною для синтезу вітаміну С (аскорбінової кислоти). Як багатоатомний спирт глюкоза реагує з купрум(ІІ) гідроксидом.
Лабораторний дослід 7
Окиснення глюкози купрум(ІІ) гідроксидом
До кількох краплин розчину купрум(ІІ) сульфату в пробірці добавте 2—3 мл розчину натрій гідроксиду. Спостерігайте утворення осаду купрум(ІІ) гідроксиду. До осаду додайте розчин глюкози й збовтайте суміш. Спостерігайте утворення прозорого розчину комплексної солі синього кольору.
Нагрійте суміш. Що спостерігаєте? Пригадайте лабораторний дослід 3 (с. 156).
Отже, залежно від умов реакції за допомогою купрум(ІІ) гідроксиду можна виявити й спиртові, й альдегідну групи в молекулі глюкози.
За наявністю гідроксильних груп можна припустити, що глюкоза здатна до реакції естерифікації. Справді, глюкоза взаємодіє з ангідридом етанової кислоти й утворює повний естер — пентаетаноат.

Важливою реакцією глюкози є реакція бродіння. Під упливом ферментів (природних каталізаторів), що їх виробляють мікроорганізми, відбувається розщеплення молекули глюкози. Зокрема, під дією ферментів дріжджів і без доступу повітря глюкоза перетворюється на етиловий спирт — відбувається спиртове бродіння.
Процеси бродіння дуже поширені у природі, залежно від кінцевого продукту є бродіння спиртове, оцтовокисле, молочнокисле та інші види. Оцтовокисле бродіння має місце під час скисання вина — утворюється етанова (оцтова) кислота (див. с. 138). Скисання молока, квашення капусти, силосування зелених кормів для худоби — все це приклади молочнокислого бродіння, у результаті якого утворюється молочна кислота.
Добування. Глюкозу добувають як продукт кислотного гідролізу полісахаридів, наприклад крохмалю.
Застосування. Вуглеводи сахароза й крохмаль під дією ферментів розщеплюються в організмі до глюкози, а вже вона окиснюється у клітинах із вивільненням енергії. Сумарно цей процес можна подати рівнянням:
![]()
Як джерело енергії глюкозу використовують у медицині для підтримання життєдіяльності виснаженого організму. Її розчин уводять прямо у кров пацієнта, оскільки саме вона переносить глюкозу до клітин організму.
Завдання для самоконтролю
1. Як ви розумієте термін вуглеводи?
2. Який зв’язок існує між назвою та смаком глюкози?
3. Які форми глюкози вам відомі? У яких агрегатних станах вони існують?
4. Чим різняться за будовою а- і β-форми глюкози?
5. Які функціональні групи визначають здатність глюкози до реакцій окиснення і відновлення, естерифікації?
6. До яких сполук окиснюється і відновлюється глюкоза?
7. У чому полягає подібність глюкози й гліцеролу; глюкози й етаналю? Як довести цю подібність експериментально?
8. Визначте окисник і відновник у реакції «срібного дзеркала».
9. Під упливом яких речовин відбувається реакція бродіння? Які продукти можуть утворитися?
10. Я ке біологічне значення реакції повного окиснення глюкози?
11. У процесі спиртового бродіння розчину глюкози утворився вуглекислий газ об’ємом 112 м3. Визначте масу безводного етанолу, що утворився.
А 230 кг
Б 112 кг
В 39,1 кг
Цей контент створено завдяки Міністерству освіти і науки України
